Soyut
Arka plan
Helicobacter pylori, gastrit, peptik ülser hastalığı ve mide kanserleri de dahil olmak üzere çeşitli üst gastrointestinal (ÜGİ) rahatsızlıklarla ilişkili önemli bir mide patojenidir. Hastalığa neden olma yeteneği büyük ölçüde sitotoksinle ilişkili gen A (cagA) ve vakuolize edici sitotoksin geni (vacA) gibi önemli virülans faktörlerinden kaynaklanmaktadır. Bu çalışma, hem fenotipik hem de moleküler yöntemler kullanarak ÜGİ semptomları gösteren hastalarda H. pylori prevalansını belirlemeyi ve izolatlarda cagA ve vacA genlerinin varlığını tespit etmeyi amaçlamıştır.
Malzemeler ve yöntemler
Semptomatik gastrointestinal (GI) şikayetleri olan ve üst GI endoskopisi geçiren hastalar çalışmaya dahil edildi. Her hastadan beyin-kalp infüzyon ortamında dört mide biyopsi örneği alındı ve mikrobiyolojik ve moleküler testler için tıbbi gastroenteroloji bölümünden gönderildi. H. pylori tanımlaması , Skirrow Campylobacter ortamı ve büyüme takviyeleri ile standart kültür teknikleri kullanılarak gerçekleştirildi. Moleküler tespit, polimeraz zincir reaksiyonu (PCR) kullanılarak yapıldı. DNA, Amp Ready reaktifi kullanılarak ekstrakte edildi ve analiz edilene kadar -20°C’de saklandı. Veriler yapılandırılmış bir form kullanılarak toplandı ve Epi Info sürüm 7.3.2 (Hastalık Kontrol ve Önleme Merkezleri (CDC), Atlanta, GA, ABD) ile analiz edildi. Kategorik değişkenler, %95 güven aralığı (CI) ile yüzdeler olarak özetlendi. İlişkiler, ki-kare testi veya Fisher’ın kesin testi kullanılarak değerlendirildi ve p ≤ 0,05 istatistiksel olarak anlamlı kabul edildi.
Sonuçlar
İşlem gören 250 mide biyopsi örneğinden 38’inde (%15,2) H. pylori kültürde üredi. ureB genini hedefleyen PCR, 36 örnekte (%14,4) H. pylori DNA’sını tespit etti. Bu PCR pozitif izolatların 30’unda (%83,3) hem cagA hem de vacA virülans genleri bulunuyordu. Genotipleme, vacA s1 ve m1 alellerinin sıklıkla bir arada bulunduğunu, s1m1 genotipinin en yaygın olduğunu ve daha yüksek virülansla ilişkili olduğunu gösterdi.
Çözüm
PCR tabanlı testlerin, H. pylori ve temel virülans belirteçlerini tespit etmede geleneksel kültür yöntemlerine kıyasla daha hassas ve etkili olduğu kanıtlanmıştır. Moleküler tekniklerin rutin tanı iş akışlarına entegre edilmesi, yüksek riskli suşların daha erken ve daha doğru bir şekilde belirlenmesini kolaylaştırabilir.
giriiş
Helicobacter pylori, mikroaerofilik koşullar altında büyüyen ve dünya nüfusunun neredeyse yarısının mide mukozasını kolonize ettiği bilinen, spiral şeklinde, gram negatif bir bakteridir. Kronik gastrit, asit peptik hastalık ve mide ülserleri de dahil olmak üzere çeşitli gastrointestinal (GI) bozukluklarla ilişkilidir ve ayrıca çeşitli mide lenfomaları türleri için bir tetikleyici olarak kabul edilmektedir [1] . Peptik ülser hastalığı ve mide kanseri ile güçlü bağlantısı nedeniyle, Dünya Sağlık Örgütü’nün (WHO) bir kolu olan Uluslararası Kanser Araştırma Ajansı (IARC), H. pylori’yi Grup I kanserojen olarak belirlemiştir [2] . Enfekte bireyler arasındaki klinik sonuçlardaki farklılıklar büyük ölçüde bakteriyel virülans faktörlerinden, özellikle de vakuolize edici sitotoksin geni (vacA), sitotoksinle ilişkili gen (cagA) ve üreaz (ure) geninden kaynaklanmaktadır [3] . Üreaz enzimi, üreyi amonyağa dönüştürerek H. pylori’yi asidik mide ortamından korumaya yardımcı olur. vacA geni tarafından kodlanan 95 kDa’lık oldukça immünojenik bir toksin olan VacA proteini, gastroduodenal hastalık şiddetinde önemli bir rol oynar. Çoğu H. pylori suşunda bulunan bu gözenek oluşturan toksin, vakuol oluşumunu indükleyerek, membran kanalları oluşturarak, sitoskelete bağlı fonksiyonları bozarak ve apoptozu teşvik ederek mide epitel hücrelerine zarar verir. Ayrıca konakçı bağışıklık tepkilerini de etkiler [3,4] . vacA geni iki değişken bölge içerir: s1a, s1b ve s2 alt tiplerine sahip sinyal (s) bölgesi ve m1 ve m2 alellerine sahip orta (m) bölge. s1/m1 ve s1/m2 kombinasyonlarını taşıyan suşlar orta ila yüksek düzeyde sitotoksik aktivite üretme eğilimindeyken, s2/m2 suşları çok az veya hiç sitotoksik aktivite üretmez [3,4] .
Cag patojenite adası (cagPAI) içinde yer alan cagA geni, CagA onkoproteinini kodlar. Tip IV salgı sistemi yoluyla mide epitel hücrelerine iletildikten sonra CagA, özellikle tirozin fosfataz SHP-2 olmak üzere konak sinyal proteinleriyle etkileşime girer. Bu etkileşim, mide karsinogenezine katkıda bulunan sitoskeletal değişikliklere ve morfolojik anormalliklere yol açar [5] .
Bu çalışmanın amacı, dispepsi şikayetiyle başvuran hastalarda H. pylori prevalansını belirlemek ve izolatların patojenik potansiyelini cagA ve vacA gibi temel virülans genlerini tespit ederek değerlendirmektir.
Malzemeler ve Yöntemler
Bu çalışma, Kalinga Tıp Bilimleri Enstitüsü (KIMS), Bhubaneswar Mikrobiyoloji Bölümü’nde, Ulusal Kolera ve Bağırsak Hastalıkları Enstitüsü (NICED), Kalküta ile işbirliği içinde yürütülmüştür. Araştırma yaklaşık iki yıl süreyle (Kasım 2013-Ağustos 2015) gerçekleştirilmiştir. Kurumsal Etik Kurulu’ndan etik onay alınmıştır (IEC onay numarası: KIMS/ETHICS/513/2013). Tüm katılımcılardan, belirlenmiş etik kurallara uygun olarak yazılı bilgilendirilmiş onam alınmıştır.
Çalışmaya katılanlar
Dahil Edilme Kriterleri
Çalışma dönemi boyunca KIMS’de gastroenteroloji polikliniğine başvuran, 18-75 yaş arası, her iki cinsiyetten yetişkinler, dispeptik semptomlar gösteren hastalar ve bireyler çalışmaya dahil edildi.
Hariç Tutma Kriterleri
Çalışmaya dispeptik semptomları olmayan hastalar, 18 yaşından küçük veya 75 yaşından büyük bireyler, son iki hafta içinde proton pompa inhibitörü (PPI) veya antibiyotik kullanımı öyküsü olanlar ve bilinen bir karsinom tanısı olan hastalar dahil edilmedi.
Örnek toplama
Endoskopi sırasında midenin antral ve gövde bölgelerinden dört adet gastrik biyopsi örneği alındı. Her örnek, hızlı üreaz testi, bakteri kültürü ve histopatolojik inceleme için ayrı ayrı işlendi. Histopatoloji için, biyopsi örnekleri %10 tamponlu formalinde sabitlendi, rutin olarak işlendi ve hematoksilin ve eozin (H&E) ve Giemsa boyalarıyla boyandı. Kültürde H. pylori’nin başarılı bir şekilde izole edildiği durumlarda, üreB, cagA ve vacA virülans genleri polimeraz zincir reaksiyonu (PCR) kullanılarak daha ayrıntılı olarak tanımlandı.
Numunenin taşınması
Alınan biyopsi örnekleri, %15 gliserol içeren 0,6 mL Brucella besiyerine (Difco Laboratories) konuldu ve toplandıktan hemen sonra buz üzerinde taşındı. Örnekler, bakteri kültürü için daha ileri işlemler yapılana kadar -70°C’de saklandı.
Mikrobiyolojik işleme
Her biyopsi örneği, Christensen’in üre suyu kullanılarak üreaz aktivitesi açısından test edildi ve uygun pozitif ve negatif kontrollerle birlikte 37°C’de bir saat inkübe edildi. Kültür için, biyopsi örnekleri iki steril cam slayt arasında ezildi ve kıyılmış doku, defibrine edilmiş at serumu (Himedia RM1239) içeren brucella agar bazı (Himedia MO74) ve Campylobacter büyüme takviyeleri (Himedia FD009 ve FD008) ile taze hazırlanmış Skirrow’un Campylobacter seçici ortamına ve ayrıca seçici olmayan bir ortam olarak çikolata agar’a aşılandı [6] .
Aşılanmış plaklar, mikroaerofilik koşullar altında 37°C’de inkübe edildi ve bakteri üremesi açısından 3-7 gün boyunca gözlemlendi. H. pylori’yi düşündüren koloniler küçük (<2 mm), dairesel, saydam ve grimsi görünümdeydi. Şüpheli izolatlar, histopatolojik bulgularla korelasyon halinde, Gram boyama (Gram negatif kavisli basiller gösteren), hareketlilik testi ve pozitif katalaz, oksidaz ve üreaz reaksiyonları ile daha da doğrulandı.
H. pylori’nin izolasyonu ve tanımlanması
Genomik DNA, setiltrimetilamonyum bromür (CTAB) yöntemi kullanılarak kültürlenmiş H. pylori izolatlarından ekstrakte edildi . Bu işlemde, bakteri hücreleri önce lizize edildi ve DNA, fenol-kloroform ekstraksiyonu ve ardından etanol çöktürmesi ile saflaştırıldı. Son DNA peletleri nükleaz içermeyen suda çözüldü ve PCR için kullanılana kadar -20°C’de saklandı.
Daha sonra, H. pylori’nin çeşitli önemli genlerini hedefleyen spesifik primerler kullanılarak PCR gerçekleştirildi . İzolatların kimliğini doğrulamak için ureB geni çoğaltıldı. Daha yüksek virülansla bağlantılı olan sitotoksinle ilişkili gen A’nın varlığını kontrol etmek için cagA geni test edildi. Ayrıca, bu alellerin farklı kombinasyonlarının toksin aktivitesini etkileyebileceğinden, vacA geninin sinyal (s) ve orta (m) bölge alellerini belirlemek için de analiz edildi.
Her PCR reaksiyonunun toplam hacmi 25 µL idi ve standart PCR tamponu (Genei, Bangalore, Hindistan), 1 U Taq DNA polimeraz, 1,5 mM MgCl₂, her bir dNTP’den 0,25 mM, her bir primerden 25 pmol ve yaklaşık 50 ng kalıp DNA içeriyordu. Amplifikasyon, Eppendorf Mastercycler kullanılarak aşağıdaki koşullar altında gerçekleştirildi: 95°C’de 1 dakika süreyle denatürasyon, 55°C’de 1 dakika süreyle bağlanma ve 72°C’de 1 dakika süreyle uzatma olmak üzere 35 döngü. Son uzatma adımı 72°C’de 10 dakika süreyle gerçekleştirildi.
PCR ürünleri, etidyum bromür (veya başka bir güvenli nükleik asit boyası) ile boyanmış %1,5’lik agaroz jel üzerinde ayrıştırıldı. Elektroforezden sonra jeller UV ışığı altında incelendi ve yükseltilmiş parçaların boyutlarını doğrulamak için 100 bp’lik bir DNA merdiveni kullanıldı.
H. pylori referans suşu ATCC 26695’ten elde edilen DNA, her PCR çalışmasında pozitif kontrol olarak kullanıldı. Kontaminasyon olmadığından emin olmak için şablon DNA olmadan kurulan reaksiyonlar negatif kontrol olarak dahil edildi. Primer dizileri [7] ve hedefledikleri genler , bu çalışmada kullanılan tüm yayınlanmış primerleri özetleyen Tablo 1’de listelenmiştir .
| Hedef gen | Astar | Sıra (5′-3′) | Amplikon boyutu (bp) |
| ureB | UreBF | CGTCCGGCAATAGCTGCCATAGT | 480 |
| UreBR | GTAGGTCCTGCTACTGAAGCCTTA | ||
| cagA | CagA5cF | GTTGATAACGCTGTCGCTTCA | 350 |
| CagA3cR | GGGTTGTATGATATTTTCCATAA | ||
| vacA (s bölgesi) | vacAs1F | ATGGAAATACAACAAACACAC | s1-259/s2-286 |
| vacAs1R | CTGCTTGAATGCGCCAAAC | ||
| vacA (m bölgesi) | vacAmF | CAATCTGTCCAATCAAGCGAG | m1-567/m2-642 |
| vacAmR | GCGTCAAAATAATTCCAAGG |
Tablo 1: Bu çalışmada kullanılan yayınlanmış primerler
Veri analizi
Toplanan veriler kodlanarak Microsoft Excel elektronik tablosuna (Microsoft Corp., Redmond, WA, ABD) girildi. İstatistiksel analiz, Epi Info sürüm 7.3.2 (Hastalık Kontrol ve Önleme Merkezleri (CDC), Atlanta, GA, ABD) kullanılarak gerçekleştirildi. Kategorik değişkenler, karşılık gelen %95 güven aralıklarıyla (CI) birlikte yüzdeler olarak özetlendi ve uygunluğa bağlı olarak ki-kare testi veya Fisher’ın kesin testi kullanılarak karşılaştırıldı. p değeri ≤ 0,05 istatistiksel olarak anlamlı kabul edildi.
Sonuçlar
Dispepsi şikayeti olan hastalardan toplam 250 mide biyopsi örneği alınarak gastroenteroloji bölümünde işleme tabi tutuldu. Bu örneklerin 38’inde (%15,2) kültür yöntemiyle H. pylori pozitifliği saptanırken, 36’sında (%14,4) ureB genini hedefleyen PCR yöntemiyle pozitiflik doğrulandı. Enfeksiyon erkeklerde (%71) kadınlara (%28) göre daha yaygındı ve en yüksek prevalans 41-50 yaş grubunda (%44,7) gözlendi (Tablo 2 ).
| Demografik değişkenler | Toplam (N = 250) | H. pylori pozitif (n = 38) | H. pylori negatif (n = 212) | Olasılık oranı (%95 güven aralığı) | p-değeri |
| Erkek | 154 | 27 | 127 | 1,64 (0,77-3,40) | 0.19 |
| Dişi | 96 | 11 | 85 | ||
| <20 yaş | 9 | 1 | 8 | 0,69 (0,08-5,67) | 0.73 |
| 21-30 yaş | 30 | 2 | 28 | 0,37 (0,08-1,60) | 0.18 |
| 31-40 yaş | 52 | 9 | 43 | 3.17 (1.75-5.73) | 0.0001 |
| 41-50 yaş | 88 | 17 | 71 | 1.61 (0.79-3.24) | 0.18 |
| 51-60 yaş | 35 | 5 | 30 | 0,91 (0,33-2,54) | 0.87 |
| 61-70 yaş | 19 | 3 | 16 | 1,05 (0,29-3,79) | 0,94 |
| >70 yaş | 17 | 1 | 16 | 0,33 (0,04-2,57) | 0.29 |
Tablo 2: Çalışma popülasyonunun temel demografik profili (N = 250)
İzole edilen 38 H. pylori suşundan 23’ü duodenum ülseri olan hastalardan, 5’i mide ülseri olan hastalardan, 8’i gastritli hastalardan ve 2’si mide karsinomlu hastalardan elde edilmiştir (Tablo 3 ).
| Endoskopik bulgular | Toplam (N = 250) | H. pylori pozitif (n = 38) | H. pylori negatif (n = 212) | Olasılık oranı (%95 güven aralığı) | p-değeri |
| Mide karsinomu | 22 | 2 | 20 | 0,53 (0,12-2,38) | 0.41 |
| Onikiparmak bağırsağı ülseri | 85 | 23 | 62 | 3.71 (1.82-7.58) | 0.0003 |
| Mide ülseri | 43 | 5 | 38 | 0,69 (0,25-1,89) | 0,48 |
| Gastrit | 61 | 8 | 53 | 0,80 (0,35-1,85) | 0,60 |
Tablo 3: Helicobacter pylori pozitifliği olan çalışma katılımcılarındaki endoskopik bulgular (N = 38)
H. pylori pozitif hastalar arasında en sık görülen semptomlar dispepsi (%24,1), ardından asit reflüsü (%23,2), hazımsızlık (%21,4), iştahsızlık (%14,2) ve epigastrik hassasiyet (%10,5) idi (Tablo 4 ).
| Belirti | Toplam vaka sayısı (n) | H. pylori pozitif (n = 38) | H. pylori negatif (n = 212) | Test istatistiği | df | p-değeri |
| Epigastrik ağrı | 38 | 4 (10.53%) | 34 (89.47%) | 0.39 | 1 | 0,53* |
| Dispepsi | 29 | 7 (24.14%) | 22 (75.86%) | 0.17 | 1 | 0,15** |
| asit reflüsü | 86 | 20 (23.26%) | 66 (76.74%) | 5.68 | 1 | 0,01* |
| İştah kaybı | 14 | 2 (14.29%) | 12 (85.71%) | 1.00 | 1 | 0,92** |
| Hazımsızlık | 14 | 3 (21.43%) | 11 (78.57%) | 0,45 | 1 | 0,50** |
Tablo 4: Hastalar arasında yaygın semptomların dağılımı (N = 250)
*Ki-kare testi. **Fisher’ın kesin testi.
Alkol tüketimi, sigara içme ve diyabetin H. pylori enfeksiyonu ile ilişkisi değerlendirildi. Alkol tüketimi enfeksiyonla anlamlı derecede ilişkiliydi ve H. pylori enfeksiyonuna yakalanma olasılığını 2,87 kat artırıyordu (p = 0,02). Sigara içme (p = 0,42) ve diyabet (p = 0,26) anlamlı bir ilişki göstermedi. Çeşitli risk faktörleri Tablo 5’te özetlenmiştir .
| Risk faktörleri | Toplam (N = 250) | H. pylori pozitif (n = 38) | H. pylori negatif (n = 212) | Olasılık oranı (%95 güven aralığı) | p-değeri |
| Alkollü | 10 | 08 | 02 | 28 (5.68-138.14) | 0,001 |
| Alkolsüz | 240 | 30 | 210 | ||
| Sigara içen | 97 | 17 | 80 | 1.33 (0.67-2.68) | 0,42 |
| Sigara içmeyen | 153 | 21 | 132 | ||
| Diyabet hastaları | 32 | 07 | 25 | 1,68 (0,67-4,2) | 0.26 |
| Diyabetik olmayanlar | 218 | 31 | 187 | ||
| HTN | 102 | 14 | 88 | 0,82 (0,40-1,68) | 0,59 |
| Hipertansiyon dışı | 148 | 24 | 124 |
Tablo 5: Helicobacter pylori enfeksiyonuyla ilişkili risk faktörlerinin analizi
PPI: proton pompası inhibitörü, HTN: hipertansiyon.
Test edilen 250 mide biyopsi örneğinden 177’si (%70,8) hızlı üreaz testi (RUT) ile pozitif, 38’i (%15,2) kültür ile pozitif ve 66’sı (%26,4) histopatoloji ile pozitif bulunmuştur. Kültürü altın standart olarak kullanarak, %100’lük bir pozitiflik oranı kaydedilmiştir (Tablo 6 ).
| Laboratuvar testleri | Pozitif örnekler, N (%) | Hassasiyet | Özgüllük | PPV | Net Bugünkü Değer (NPV) |
| Hızlı üreaz testi | 177/250 (70.80) | %100,00 | %34,43 | %21,47 | %100,00 |
| Histoloji | 66/177 (37.30) | %100,00 | %86,79 | %57,58 | %100,00 |
| PCR (ureB geni) | 36/38 (94.70) | %94,74 | %100,00 | %94,74 | %99,07 |
Tablo 6: Helicobacter pylori’yi tespit etmede çeşitli tanı testlerinin özgüllüğü ve duyarlılığı
PCR: polimeraz zincir reaksiyonu, ureB geni: üreaz B geni, PPV: pozitif tahmin değeri, NPV: negatif tahmin değeri.
Test edilen 250 örneğin 36’sında (%14,4) ureB genini hedefleyen PCR ile H. pylori pozitifliği saptandı (Tablo 6 , Şekil 1 ). Bu 36 PCR pozitif izolatın 30’unda (%83,3) hem cagA hem de vacA genleri pozitif bulundu (Tablo 7 , Şekil 2 ).
| Endoskopik bulgu | Toplam vaka sayısı (n) | cagA/vacA-pozitif (n = 30) | cagA/vacA-negatif (n = 6) | Test istatistiği | df | p-değeri |
| Mide karsinomu | 2 | 2 (100.00%) | 0 (0.00%) | 1.00 | 1 | 1,00** |
| Onikiparmak bağırsağı ülseri | 22 | 19 (86.36%) | 3 (13.64%) | 0,02 | 1 | 0,89* |
| Mide ülseri | 5 | 4 (80.00%) | 1 (20.00%) | 1.00 | 1 | 1,00** |
| Gastrit | 7 | 2 (28.57%) | 5 (71.43%) | 0.0003 | 1 | 0,07** |
Tablo 7: 36 Helicobacter pylori pozitif hastada sitotoksinle ilişkili gen A (cagA) ve vakuolize edici sitotoksin geni (vacA) ile endoskopik bulgular arasındaki ilişki
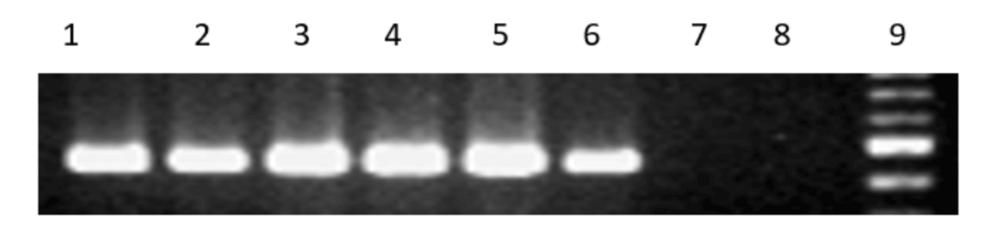
Şekil 1: Helicobacter pylori’nin ureB geninin PCR ile çoğaltılması
Şerit 1: pozitif kontrol. Şeritler 2-7: klinik izolatlar. Şerit 8: Escherichia coli DNA’sı (negatif kontrol). Şerit 9: 100 bp DNA merdiveni (moleküler ağırlık belirteci). Beklenen amplikon boyutu 480 bp idi. Kültür pozitif 38 H. pylori izolatından 36’sı (%94,7) ureB pozitif iken, 2 negatif örnek daha ileri analizlerden çıkarıldı.

Şekil 2: Virülans genlerinin (cagA ve vacA) moleküler karakterizasyonu
(A) cagA geninin amplifikasyonu, cagA pozitif izolatlar için 350 bp’lik ve cagA negatif izolatlar için 550 bp’lik bir ürün göstermektedir. (B) vacA geninin amplifikasyonu, s bölgesi için 259 bp’lik ve m bölgesi için 567 bp’lik bir ürün göstermektedir. 36 ureB pozitif izolatın 30’u (%83,3) hem cagA hem de vacA genleri için pozitifti. vacA’nın toksik alleli s1m1, tüm vacA pozitif suşlarda mevcuttu.
cagA: sitotoksinle ilişkili gen A, vacA: vakuol oluşturan sitotoksin geni.
cagA ve vacA virülans genleri, mide karsinomu vakalarının %100’ünde, duodenum ülseri vakalarının %86,3’ünde, mide ülseri vakalarının %80’inde ve gastrit vakalarının %71,4’ünde tespit edildi (Tablo 8 ).
| Endoskopik bulgu | Toplam vaka sayısı (n) | cagA/vacA-pozitif (n = 30) | cagA/vacA-negatif (n = 6) | Test İstatistiği | df | p-değeri |
| Mide karsinomu | 2 | 2 (100.00%) | 0 (0.00%) | 1.00 | 1 | 1,00** |
| Onikiparmak bağırsağı ülseri | 22 | 19 (86.36%) | 3 (13.64%) | 0,02 | 1 | 0,89* |
| Mide ülseri | 5 | 4 (80.00%) | 1 (20.00%) | 1.00 | 1 | 1,00** |
| Gastrit | 7 | 2 (28.57%) | 5 (71.43%) | 0.0003 | 1 | 0,07** |
Tablo 8: Helicobacter pylori suşlarında (n = 36) cagA ve vacA virülans genlerinin endoskopik bulgularla ilişkisi
*Ki-kare testi. **Fisher’ın kesin testi.
cagA: sitotoksinle ilişkili gen A, vacA: vakuol oluşturan sitotoksin geni.
36 ureB pozitif izolatın 30’u (%83,3) cagA ve vacA pozitifti (Tablo 9 ).
| Endoskopik bulgular | vacA-pozitif | vacA s1 | vacA s2 | vacA m1 | vacA m2 |
| Mide karsinomu | 2 | Pozitif | Negatif | Pozitif | Negatif |
| Onikiparmak bağırsağı ülseri | 19 | Pozitif | Negatif | Pozitif | Negatif |
| Mide ülseri | 4 | Pozitif | Negatif | Pozitif | Negatif |
| Gastrit | 5 | Pozitif | Negatif | Pozitif | Negatif |
Tablo 9: Hastalardan alınan Helicobacter pylori izolatlarında vacA allelik varyantlarının PCR tabanlı tespiti (n = 36)
vacA s1: vakuol oluşturan sitotoksin A geni, sinyal bölgesi tipi s1, vacA s2: vakuol oluşturan sitotoksin A geni, sinyal bölgesi tipi s2, vacA m1: vakuol oluşturan sitotoksin A geni, orta bölge tipi m1, vacA m2: vakuol oluşturan sitotoksin A geni, orta bölge tipi m2.
Kültür testi pozitif çıkan 38 H. pylori izolatından 36’sı (%94,7) ureB pozitifti. Negatif çıkan iki örnek çalışmadan çıkarıldı.
Tartışma
H. pylori gastrit, peptik ülser hastalığı ve mide kanserlerinden sorumlu önemli bir patojendir. Enfeksiyonun yaygınlığı yaş, cinsiyet, beslenme alışkanlıkları ve genetik yatkınlık gibi faktörlere göre değişmektedir [8] .
Bu çalışma , semptomatik hastalarda üst gastrointestinal endoskopi sırasında H. pylori enfeksiyonunun yaygınlığını belirlemeyi ve beslenme alışkanlıkları, sigara ve alkol tüketimi gibi ilişkili risk faktörlerini araştırmayı amaçlamıştır . Ek olarak, izole edilen H. pylori suşlarının patojenik potansiyeli, cagA ve vacA virülans genlerinin varlığının saptanmasıyla değerlendirilmiştir.
H. pylori enfeksiyonunun yaygınlığı , yoksulluk, aşırı kalabalık, yetersiz sanitasyon ve kötü hijyen gibi sosyoekonomik faktörler nedeniyle ülkeler arasında ve hatta aynı ülkenin bölgeleri içinde bile büyük farklılıklar göstermektedir. Aynı nüfus içindeki çeşitli etnik gruplar arasında da farklılıklar gözlemlenmektedir [9] .
Namyalo ve diğerleri, H. pylori’nin yaygınlığının gelişmekte olan ülkelerde, özellikle Afrika gibi kaynak kısıtlı ortamlarda %70 civarında olduğunu, gelişmiş ülkelerde ise %25 ile %40 arasında değiştiğini bildirmiştir [10] .
Hindistan’da yapılan çalışmalar sırasıyla %62,7, %72,8, %83,5 ve %35,6 oranlarında yaygınlık oranları bildirmiştir [11-14] . Buna karşılık, bizim çalışmamızda genel yaygınlık oranı %15,2 olarak bulunmuştur. Bölgemizdeki nispeten düşük yaygınlık oranı, sosyoekonomik durum, sanitasyon ve su temini gibi çevresel faktörlerin yanı sıra etnik köken, yaş ve ırk gibi konakçı faktörlerinin bir kombinasyonunu yansıtıyor olabilir.
Çalışmamızda en yüksek yaygınlık (%19,3) 41-50 yaş grubunda gözlemlenmiştir. Vadivel ve ark. [11] , Hindistan’ın güneyindeki Chennai’de, en yüksek yaygınlığı (%58,1) 21-39 yaş grubunda bildirmiş olup, bu da H. pylori yaygınlığının topografik, kültürel ve davranışsal faktörlerden etkilendiğini göstermektedir. Çalışmamızda 41-50 yaş grubundaki daha yüksek yaygınlık, iş, mali yükümlülükler ve kişisel veya ailevi sorumluluklarla ilişkili stres ve kaygı ile ilgili olabilir. Adlekha ve ark. [8] tarafından bildirildiği üzere, stres, kaygı ve depresyon gibi psikolojik faktörlerin H. pylori enfeksiyonunu önemli ölçüde etkilediği gösterilmiştir .
Çalışmamızda, H. pylori enfeksiyonunun yaygınlığı erkeklerde (%59,9) kadınlara (%40,1) göre daha yüksekti; bu, Bharati ve diğerlerinin [9] bulgularıyla tutarlıdır .
Ek olarak, çalışmamızdaki duodenal ülser vakalarının %25,8’inde kültürde H. pylori pozitifliği saptandı; bu istatistiksel olarak anlamlı bir ilişkidir (P < 0,05). Bu, Cekin ve ark. tarafından yapılan çalışmayla örtüşmektedir; bu çalışmada H. pylori, hastaların %84,9’unda duodenal ülser hastalığının patogenezinde rol oynamış ve vakaların %44,1’inde tek nedensel faktör olarak belirlenmiştir [15] .
Bu çalışmada analiz edilen çeşitli risk faktörleri arasında, yalnızca alkol tüketimi H. pylori enfeksiyonu ile istatistiksel olarak anlamlı bir ilişki göstermiştir (p = 0.0001). Hem sigara içmenin hem de alkol alımının mide mukozasının bütünlüğünü bozduğu, böylece H. pylori’nin kolonizasyonunu kolaylaştırdığı ve peptik ülser hastalığı ve mide kanseri de dahil olmak üzere ilgili durumlara katkıda bulunduğu bilinmektedir. Bu bulgu, yaşam tarzı risk faktörlerine sahip bireyler arasında H. pylori enfeksiyonunun yüksek prevalansını bildiren Bharati ve ark. ile tutarlıdır ; sigara içenlerin %62,5’i ve alkol tüketenlerin %60,7’si bakteri için pozitif test sonucu vermiştir [9] .
H. pylori enfeksiyonu tipik olarak mide iltihabına neden olur ve semptomların varlığı ve şiddeti genellikle enfeksiyon durumunu yansıtır. Ali ve ark. tarafından yapılan bir çalışma, epigastrik ağrı, yanma hissi ve H. pylori pozitifliği arasında anlamlı bir ilişki olduğunu göstermiştir [16] . Mevcut çalışmada, enfekte hastalarda en sık bildirilen semptom dispepsi (%24,1) olup bunu asit reflüsü (%23,2), hazımsızlık (%21,4), iştahsızlık (%14,2) ve epigastrik hassasiyet (%10,5) izlemiştir.
Bu çalışmada, 250 dispeptik hastanın 177’sinde (%70,8) RUT pozitif bulunmuştur. Bu RUT pozitif hastaların 66’sında (%37,3) histolojik inceleme ile pozitiflik doğrulanmıştır. 177 hastanın 38’inde (%21,5) kültür pozitifliği gözlemlenmiş olup, bunların 36’sında (%94,7) ureB genini hedefleyen PCR ile de pozitif sonuç elde edilmiştir. Kültürün nispeten düşük duyarlılığı, olumsuz koşullar altında (örneğin, oksijen maruziyeti) bakteriyel canlılığın azalması, biyopsi örneklerinde düşük bakteri yükü, kokoid formların varlığı ve H. pylori’nin kültürlenmesindeki zorluk gibi birçok faktöre bağlanabilir . Ayrıca, hastanın daha önce PPI veya antibiyotik kullanması da kültür duyarlılığını daha da tehlikeye atabilir [6] .
Buna rağmen, kültür, RUT ve histolojiye kıyasla %100 özgüllük ve %100 pozitif prediktif değer (PPV) göstermiştir. Bu bulgular, H. pylori’nin kültür tabanlı tespiti için %100 özgüllük ve PPV bildiren önceki çalışmalarla tutarlıdır [17-19] . Benzer şekilde, Mutita ve ark. gerçek zamanlı PCR kullanarak %84,8 ve kültür ile %19,5 oranında bir prevalans bildirmiş ve moleküler yöntemlerin geleneksel kültüre göre daha yüksek duyarlılığını vurgulamıştır [20] .
Hindistan’da H. pylori için kültür pozitiflik oranları önemli ölçüde değişkenlik göstermektedir. Sharma ve ark. ile Chyne ve ark. tarafından yapılan çalışmalar sırasıyla %4,2 ve %3,3 gibi düşük izolasyon oranları bildirirken, Parimala ve ark. %52,45 gibi çok daha yüksek bir oran kaydetmiştir [18,21,22] . Bu farklılıklar, biyopsi örneklerinin kalitesi, bakteri yükü, kokoid formların varlığı, örnek işleme ve laboratuvar tekniklerindeki farklılıklar gibi canlı organizmaların geri kazanımını etkileyebilecek faktörlere bağlanabilir.
cagA, patojeniteyi artıran ve enfekte hastalarda mide karsinomu ve tedavi direnci riskinin artmasıyla ilişkili olabilen önemli bir virülans faktörüdür. H. pylori genetik olarak çeşitli bir patojendir ve cagA pozitif suşların yaygınlığı coğrafi olarak değişmektedir. Bu çalışmada, izolatların %83,39’u cagA pozitifti; bu oran Meksika, İran, Irak ve Bangladeş’ten gelen raporlarla karşılaştırılabilir düzeydedir. Bu oran, genellikle %60 civarında olan Filistin, Küba, Avrupa, Venezuela, Kuzey Amerika ve Pakistan’da bildirilen yaygınlık oranlarından daha yüksek, ancak cagA pozitifliğinin %90’ı aştığı Japonya ve Kore’deki oranlardan daha düşüktür [23-24] . Jeyamani ve ark. benzer şekilde, Doğu Asya’da cagPAI yaygınlığının yaklaşık %60 olduğunu, Hindistan’da ise %90’a kadar çıktığını ve Batı popülasyonlarından önemli ölçüde daha yüksek olduğunu bildirmiştir [25] .
Çalışmamızda, hem cagA hem de vacA virülans genlerinin prevalansı %83,3 olup, en yüksek pozitiflik oranı mide karsinomlu hastalarda (%100), ardından duodenum ülserli hastalarda (%86,3), mide ülserli hastalarda (%80) ve gastritli hastalarda (%71,4) gözlemlenmiştir. Bu yüksek cagA prevalansı, Patra ve ark. tarafından bildirilen %92,3’lük prevalans oranı gibi önceki bulgularla tutarlıdır [26] .
Mutita ve ark. cagA- ve vacA-pozitif H. pylori suşlarının sırasıyla %52,6 ve %5,3 oranında olduğunu ve ağırlıklı olarak mide kanseri olan hastalarda tespit edildiğini bildirmiştir. cagA-pozitif suşların, mide epitel hücrelerine daha güçlü yapışma gösterdiği ve cagA-negatif suşlara göre daha belirgin pro-enflamatuar yanıtlar indüklediği bulunmuştur [20] .
Bu çalışmada, cagA pozitif olan H. pylori örneklerinin %83,3’ünde vacA s1m1 alleli tespit edilmiştir. H. pylori vacA genotipleri dört ana kombinasyona ayrılabilir: s1m1, s1m2, s2m1 (nadir) ve s2m2. Bunlar arasında, s1m1 suşları mide epitel hücrelerinde en yüksek vakuolize edici sitotoksin aktivitesiyle, s1m2 suşları orta düzeyde aktiviteyle ve s2m2 suşları minimal veya hiç sitotoksisite göstermemektedir [3,4] . Özellikle, pozitif vakalarımızda, %80’i (72/90) cagA genini taşıyordu. vacA’nın sinyal (s) bölgesi için, izolatların %98,8’i (83/84) s1 iken, %1,2’si (1/84) s2 idi. Orta (m) bölge için %63,6’sı (56/88) m1, %2,3’ü (2/88) m2 ve %34,1’i (30/88) hem m1 hem de m2 alellerini taşıyordu; bu, Brasil-Costa ve ark. [27] tarafından bildirilen bulgularla tutarlıdır . Kishk ve ark. ayrıca vacA+/cagA+ s1m1 genotipinin en sık görülen genotip olduğunu ve peptik ülser hastalığı, gastrit ve gastroözofageal reflü hastalığı ile güçlü bir şekilde ilişkili olduğunu bildirmiştir [28] .
Çalışmanın sınırlılıkları
Bu çalışma H. pylori’nin yaygınlığına ve temel virülans genlerinin (cagA ve vacA) dağılımına odaklanırken , gelecekteki araştırmalar kapsamı antimikrobiyal duyarlılık testini de içerecek şekilde genişletebilir.
Sonuçlar
Bu çalışmada gözlemlenen H. pylori enfeksiyonunun yaygınlığı, daha önceki Hint çalışmalarında bildirilenlerden daha düşüktü ve pozitif vakaların çoğunluğu duodenum ülserleriyle ilişkiliydi. Alkol tüketimi, sigara içme ve diyabet gibi risk faktörleri, enfeksiyon olasılığının artmasıyla önemli ölçüde ilişkiliydi. Özellikle, izolatların yüksek bir oranı, peptik ülser hastalığıyla güçlü bir şekilde bağlantılı olan ve mide kanserine katkıda bulunma potansiyeli taşıyan cagA geni için pozitifti. Bu, incelenen popülasyonun ciddi gastroduodenal komplikasyonlar açısından daha yüksek risk altında olabileceğini göstermektedir. İlgili semptomlar ve ilişkili risk faktörleri gösteren hastalarda hedefli tarama, cagA pozitif suşların erken teşhisini kolaylaştırabilir ve hastalık ilerlemesini, morbiditeyi ve mortaliteyi önlemek için zamanında müdahale sağlayabilir. Bu nedenle, uygun tedaviyi yönlendirmek ve başarılı eradikasyonu doğrulamak için H. pylori enfeksiyonu olan hastalarda rutin cagA taraması yapılmasını öneriyoruz.