Tedavisi zor çocukluk çağı kanserlerinden sorumlu olanlar da dahil olmak üzere hastalığa neden olan proteinleri ortadan kaldıran PROTAC tedavileri için momentum inşa ediyor.

Üç yaşındayken Evan Lindberg’e, beyin dışındaki sinir dokusunda gelişen bir çocukluk kanseri olan nöroblastoma teşhisi kondu. O zamana kadar tümörler küçük vücuduna yayılmıştı. Bunu kemoterapi, radyasyon, immünoterapi ve çoklu ameliyatlar izledi. Evan’ın babası Gavin, “Dört yıl boyunca oğlumun hiç izin günü olmadı,” diyor. “Ya tedavi görüyordu ya da iyileşiyordu. Ve sık sık iyileşme tedaviden daha kötüydü.” Evan 2010 yılında yedi yaşında öldü.
Evan’ın doktorlarından biri olan Philadelphia, Pennsylvania Çocuk Hastanesi’nden pediatrik onkolog Yael Mossé, uzun zamandır gelişmiş tedavi seçenekleri arıyor. Yirmi yıldan fazla bir süredir nöroblastoma üzerinde çalışıyor, ancak küçük ilerlemelere rağmen “daha rasyonel veya hedefli tedaviler geliştirmede gerçekten çok az ilerleme kaydettik” diyor. Bu genel olarak çocukluk çağı katı tümörleri için geçerlidir. Bu tür tümörler çocuklarda kan kanserlerinden daha az yaygın olsa da, Amerika Birleşik Devletleri’nde 0-14 yaş arası1 çocuklarda kanserle ilişkili ölümlerin yarısından fazlasını oluştururlar. Bu çocukluk çağı kanserleri biyolojilerinde yetişkin kanserlerden farklıdır ve bu nedenle farklı tedaviler gerektirir. Yine de 2000’den bu yana ABD Gıda ve İlaç İdaresi’nden (FDA) onay alan 180’den fazla kanser ilacından bir düzineden azı özellikle çocuklar için geliştirilmiştir.
Mossé şimdi umutlarını hücrenin protein bertaraf makinesini ele geçiren laboratuvarda üretilen moleküllere bağlıyor. Tipik ilaçlar, aktivitesini engellemek için bir proteinin iş ucunu sartır.
Proteoliz hedefleyen kimeraların kısaltması olan PROTAC’lar, proteini tamamen ortadan kaldırır. Bunu, insan hücrelerindeki hastalıkla ilişkili proteinleri, proteini imha için etiketleyen bir enzime bağlayarak yaparlar.
İngiltere’deki Dundee Üniversitesi’nden biyokimyacı Alessio Ciulli’nin bir protein “ölüm öpücüğü” olarak adlandırdığı bu kader karşılaşmalarını mümkün kılmak, olası ilaç hedeflerinin listesini genişletiyor. Örneğin, kansere ve diğer hastalıklara neden olduğu bilinen yaklaşık 3.000 proteinden, FDA tarafından onaylanan ilaçlar 700’den azını hedefliyor. Geri kalanların çoğu “uyuşturulamaz” olarak kabul edilir, çünkü bir ilacın proteinin aktivitesini bağlayabileceği ve engelleyebileceği uygun bir cep yoktur. Ancak bir PROTAC’ın sadece kavraması gerekiyor; gerisini hücrenin mevcut makineleri yapıyor.
İnsanlarda, özellikle kanser, aynı zamanda Parkinson hastalığı, enflamatuar bozukluklar ve ağrı için testlerin başladığı 2019’dan bu yana en az 30 PROTAC klinik çalışmalara girdi. En gelişmiş üç meme kanseri, prostat kanseri ve lösemi, pazar onayından önceki son adım olan faz III denemelerindedir. Zaten onaylanmış ilaçlar tarafından hedeflenen proteinlerin çoğu bozunur.

Mossé ve meslektaşları, daha önce hiç ilaçlanmamış kanser proteinlerinin peşinden çalarak farklı ve daha riskli bir şey yapıyorlar. Nöroblastom ve beyin, karaciğer ve kemik kanserleri de dahil olmak üzere diğer çocukluk kanserlerinden sorumlu ilaçsız proteinlere karşı PROTAC’lar geliştiren bir ekibe liderlik ediyor. Tüm kanserler katı tümörler oluşturur. Mossé, ekibin ilk PROTAC’larının önümüzdeki birkaç yıl içinde klinik denemelere girmesini bekliyor.
Diğer araştırmacılar da benzer şekilde, kanserde ve ötesinde uzun zamandır dokunulmaz olarak kabul edilen proteinleri parçalamayı hedefliyorlar. Watertown, Massachusetts’te bir protein bozunma ilaç şirketi olan C4 Therapeutics’in kurucu ortağı olan Kaliforniya’daki Stanford Üniversitesi’nden kimyager Nathanael Gray, “Bu teknolojiyle yepyeni bir şeyi hedefleyebileceğinizi göstermek, alan için çok önemli bir an olacaktır” diyor.
Bir laboratuvar hilesinden daha fazlası
İlk çalışan PROTAC, 2001 yılında, New Haven, Connecticut’taki Yale Üniversitesi’nde kimyasal bir biyolog olan Craig Crews, Pasadena’daki California Teknoloji Enstitüsü’nden biyokimyacı Raymond Deshaies ve meslektaşları, hücre sıvısındaki hedef proteinini kurbağa yumurtalarından bozan bir tane inşa ettiğinde gösterildi2. O zamanlar, çoğu bilim insanı PROTAC’ları bir laboratuvar hilesi olarak görüyordu. Ciulli 2009’da onlarla çalışmaya başladığında, meslektaşları “gözlerini devirdi” diye hatırlıyor. “‘PROTAC’lar mı? Asla uyuşturucu olmayacaklar.'”
İlk engellerden biri, PROTAC’ları hücrelere nüfuz edecek kadar küçük yapmaktı. Bir diğeri, onları ubiquitin ligazları olarak bilinen enzimlerin en bol ve verimli olanlarını ele geçirecek şekilde tasarlamaktı. Yaklaşık 600 çeşidi olan bu enzimler, ubiquitin adı verilen çok daha küçük proteinlerden oluşan zincirler ekleyerek proteinleri imha için etiketler (bkz. ‘Protein ortadan kaldırıldı’). Büyük bir çabadan sonra, 2015’te üç makale, hücrelerdeki ve farelerdeki hedef proteinleri neredeyse tamamen ortadan kaldıran güçlü PROTAC’ları ortaya çıkardı3-5. Ciulli, “Bu makalelerden sonra proteinleri parçalayabileceğimize dair hiçbir şüphe yoktu” diyor. “Şimdi tüm hedefler dünyası açılabilir.” Makalelerden birinin ortak yazarı olan Ciulli, daha sonra Cambridge, Birleşik Krallık’ta bir protein bozunma şirketi olan Amphista Therapeutics’in kurulmasına yardımcı oldu.
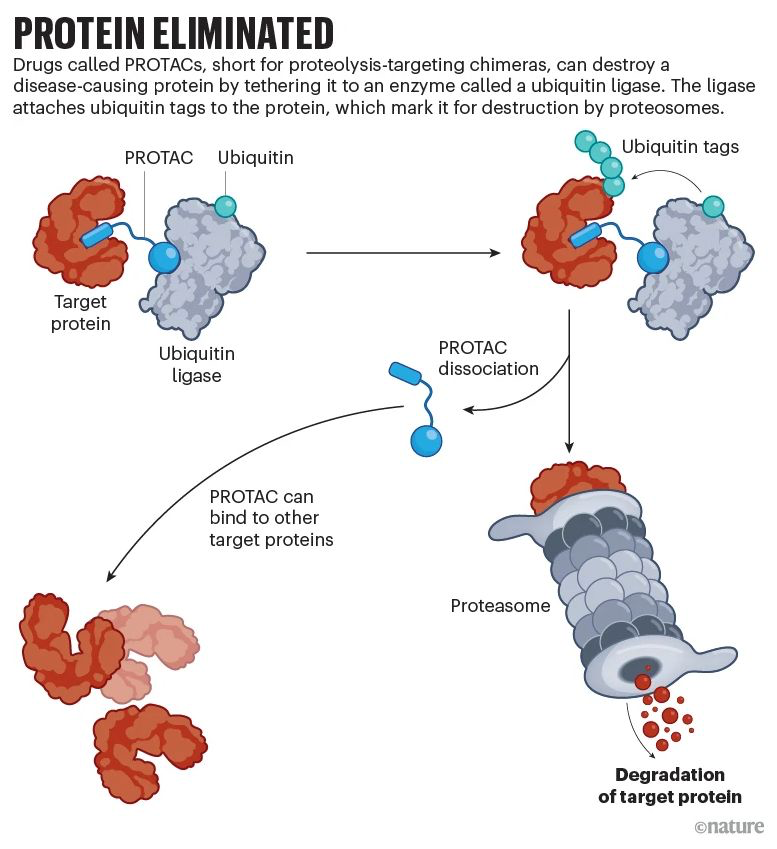
Makaleler, PROTAC’ların önemli bir avantajını vurguladı. Geleneksel ilaçların hastalığa neden olan bir proteine yerleşmesi gerekirken, PROTAC’lar hedefleriyle kısa bir süre etkileşim kurar, onu imha için gönderir ve bir sonraki hedefe geçer. Bu yakala ve bırak özelliği, çok küçük dozların uzun süre dayanabileceği anlamına gelir. Diğer bir avantaj, PROTAC’ların esir almamasıdır. Bazı proteinler bir hastalığa birden fazla şekilde katkıda bulunur, ancak bir PROTAC proteini tamamen yok ederek olası tüm katkıları ortadan kaldırır.
2015 makaleleri, PROTAC’ları bir sonraki ilaç dalgası olarak kurdu. Gray, “Bu kadar hızlı bir şekilde daha yaygın olarak benimsenen bir teknoloji görmedim” diyor. “Bu sadece küçük riskli biyoteknolojiler değil. Tüm ilaç şirketlerinin gelişmiş bozunma programları vardır.”
Bunların hepsi Evan Lindberg için çok geç oldu. 2010 yılında babası onu Mossé’nin klinik denemelerinden birine dahil etti ve mevcut bir ilacı nöroblastomda sıklıkla bozulmuş bir proteine karşı test etti. Evan’ın kanseryanıt vermedi. Tümör ayrıca, çocukluk çağı kanserlerinin kötü şöhretli bir itici gücü olan bir protein olan transkripsiyon faktörü MYCN için genin ekstra kopyalarını içeriyordu. MYCN, çocukluk gelişimi sırasında hücrelerin çoğalmasını sağlamak için genleri açar. Çok fazla, kontrolsüz büyüme yoluyla aksi takdirde tedavi edilebilir kanserleri agresif katillere dönüştürebilir. Ancak MYCN gibi transkripsiyon faktörleri ilaçsız olarak kabul edilir.
2019’da MYCN ile ilgili bir toplantıda Mossé, PROTAC’ların bir çözüm olabileceğini fark etti. Mossé, San Francisco, Kaliforniya’daki PROTAC şirketi Nurix Therapeutics’in kurucularından birinin toplantıya katıldığını ve “hedeflenen protein bozunması hakkında düşünmemiz ve gerçekten büyük bir şey yapmaya çalışmak için MYCN’nin peşinden gitmemiz için bizi gerçekten motive ettiğini” söylüyor. Özel bir vakıf hibesi ile donanmış, Nurix ile çalışmaya başladı. Çalışma, Almanya’daki Würzburg Üniversitesi’nden biyokimyacı Martin Eilers ile birlikte bir araya gelen bir Mossé ekibinin çocukluk çağı katı tümörleriyle mücadele etmek isteyen küresel bir kar amacı gütmeyen girişim olan Cancer Grand Challenges’tan büyük bir hibe kazanmasıyla 2024’te genişledi.
Onkojenik Sürücüleri Nakavt Etmek ve Çocukluk Çağı Kanserlerini Tedavi Etmek için KOODAC adlı ekip, Birleşik Krallık, Avusturya ve Fransa’daki bilim insanlarını ve beş kıtada hasta savunucularını da içeriyor. Bunlar arasında, Evan’ın ölümünden sonra, son on yıldır Mossé’nin laboratuvarında bir araştırma pozisyonu finanse eden bir hayır kurumu kuran Gavin Lindberg ve eşi Wendy de var. Ekip, MYCN ve diğer dört protein hedefinin peşinden gidiyor. Amaç, sadece işe yarayan değil, aynı zamanda hastane infüzyonlarından daha uygun ve ailelerin genellikle maliyet nedeniyle tedaviden vazgeçmek veya tedaviyi bırakmak zorunda kaldığı düşük ve orta gelirli ülkelerde satın alınabilecek kadar ucuz olan ilaçlar bulmaktır.
Çocukluk katillerini öldürmek
KOODAC ekibinin hedeflediği proteinlerden üçü, genellikle kanserde bulunan bir tür genetik hatadan kaynaklanmaktadır. Kromozomların çaprazlanması, kırılması ve onarılması, her iki orijinal genden de dizilere sahip yeni bir hibrit gene – bir gen füzyonuna – yol açabilir. Ortaya çıkan füzyon proteinleri, birçok lösemi, lenfoma ve çocukluk çağı katı tümörlerinin doğrudan nedenidir. Bu füzyon proteinlerinden ikisi Ewing sarkomunu ve rabdomyosarkomunu yönlendirerek çocukluk çağı kemik ve yumuşak doku kanserlerini tahrip eder. Üçüncüsü nadir görülen bir karaciğer kanserine neden olur.
St.’de bir hematolog olan Charles Mullighan, tümör hücreleri geliştikçe füzyon proteinlerinin devam ettiğini ve bu da onları çekici hedefler haline getirdiğini söylüyor. Memphis, Tennessee’deki Jude Çocuk Araştırma Hastanesi. Mullighan ve meslektaşları, çocukluk çağı kan kanserleri ve beyin tümörleri için PROTAC’lar ve benzer protein bozunurları yapar ve test eder. Mullighan, protein parçalayıcılarının bu kanserleri iyileştirip iyileştiremeyeceğine gelince, “potansiyel var” diyor. Ancak bir ilacın yeterli olmayabileceğini de ekliyor. “Kanserler kurnazdır ve bunun etrafında yollar bulabilirler.”
KOODAC’a ek olarak, diğer iki Cancer Grand Challenges ekibi çocukluk çağı katı tümörleriyle mücadele ediyor. Bir ekip, protein bozunucuları ve hücre tedavileri üzerinde çalışmak için Avrupa ve Amerika Birleşik Devletleri’ndeki dokuz kurumdan araştırmacıları bir araya getiriyor. Amerika Birleşik Devletleri, Birleşik Krallık ve Fransa’daki sekiz kurumdaki araştırmacıları içeren diğeri, yalnızca hücre tedavilerine odaklanmıştır. Araştırmacılar, çocukluk çağı kanserleri konusunda ilerleme kaydetmek için bu kadar geniş akademik işbirliklerinin gerekli olduğunu söylüyor. Hücre terapisi ekibinin eş lideri ve Washington DC’deki Ulusal Çocuk Hastanesi’nde pediatrik hematolog olan Catherine Bollard, “Sadece pediatrik kanserler için pazar o kadar küçük ki, geleneksel bir ilaç şirketinin ticarileştirme planına uymuyor” diyor.
PROTACtable evren
Henüz hiçbir PROTAC onaylanmadı. New Haven, Connecticut’ta Arvinas tarafından geliştirilen faz III denemelerine giren ilk vepdegestrant, çoğu meme kanserinin büyüme için güvendiği östrojen reseptörünü bozar. Mart ayı başlarında, Arvinas ve ortağı Pfizer, tümörleri genellikle meme kanseri ile ilişkili bir mutasyona sahip olan deneme katılımcılarının hastalık kötüleşmeden daha uzun yaşamalarını sağlamada bozurucunun standart bir anti-östrojen ilacından daha iyi olduğunu bildirdi (tüm deneme katılımcılarını içeren bir analizde daha iyi performans göstermedi). Arvinas baş sağlık sorumlusu Noah Berkowitz, Nature’a gönderdiği bir e-postada, “Düzenleyici dosyaları potansiyel olarak desteklemek için [deneme] verilerini küresel düzenleyici otoritelerle paylaşmayı planlıyoruz” dedi. Diğer iki vepdegestrant faz III denemesi devam ediyor.
Bu arada, diğer iki PROTAC faz III denemelerine ulaştı. Biri çoğu metastatik prostat kanserini yönlendiren androjen reseptörünü bozar; diğeri, kronik lenfositik lösemilerin gerektirdiği BTK enzimi. Bu hedeflere karşı ilaçlar zaten mevcuttur, ancak ileri kanserler kaçınılmaz olarak bunlara dirençli hale gelir.
Sözlerine rağmen, PROTAC’lar sınırlamalarla birlikte gelir. Hücre zarına gömülü proteinlere bağlanmakta zorlanırlar ve hücre dışındaki proteinleri parçalayamazlar. Ayrıca tüm proteinleri ortadan kaldırmanın bilinmeyen riskleri ve beklenmedik proteinlerin bozulacağına dair endişeler de vardır. Sinovyal sarkomlu kişilerde BRD9 adı verilen bir proteine karşı ilaçsız proteinler için geliştirilen ilk PROTAC’lardan ikisi rafa kaldırıldı – ilki FDA’nın kardiyak toksisite nedeniyle denemeyi duraklatmasından sonra ve ikincisi ilacın yeterince etkili olmadığı için
İlk PROTAC onayı önemli bir adım olacaktır, ancak diğer ilaçlar tarafından zaten hedeflenen kanserle ilişkili bir protein için olması muhtemeldir. Kaliforniya, Thousand Oaks’taki Amgen’de protein parçalayıcı programınaliderlik eden Ryan Potts, daha önce ilaçlanmamış proteinleri hedeflemenin “gerçek atılım anı” olacağını söylüyor. “En büyük kazanımlar oradan gelebilir.”
Geçen yıl, Watertown’da Kymera Therapeutics tarafından geliştirilen bir PROTAC için klinik çalışmalar başladı. Bu PROTAC, alerjik ve enflamatuar hastalıklarda yer alan ilaçsız bir transkripsiyon faktörü olan STAT6’yı hedeflemektedir. Kymera baş sağlık sorumlusu Jared Gollob, hem etkili hem de güvenli olması gerektiğini söylüyor. Aynı yoldaki diğer proteinler zaten başarılı bir şekilde hedeflenir, hafif yan etkilere neden olur ve STAT6’sı olmayan fareler sağlıklıdır6. Gollob, “Güvenlik sonuçları olmadan hedefi sert bir şekilde vurabilmeliyiz” diyor.
Hücrelerin içindeki ilaçlanması zor proteinlerin neredeyse her hastalıkta rolleri vardır. Örneğin, Alzheimer, Parkinson ve motor nöron hastalığı gibi hastalıklarda düzgün bir şekilde katlanamayan ve bir araya gelemeyen “bozuk” proteinler zor kalmıştır. PROTAC’lar kümeleri kolayca temizleyemese de, onları tohumlayan anormal proteinleri ortadan kaldırabilirler. Örneğin Arvinas, Alzheimer ve Parkinson hastalığında yer alan tau ve α-sinüklein proteinlerinin yanı sıra Huntington hastalığındaki mutant huntingtin proteininin formları için PROTAC bozunucuları geliştiriyor.
Gray, protein bozunucularının immünoterapi veya gen terapisine benzer bir ölçekte önemli bir ilaç kategorisi haline geldiğini görmeyi bekliyor. “Sadece kanserde değil, birden fazla düzenleyici onay olacağından çok az şüphem var” diyor.
PROTAC’ların yanı sıra ekipler, moleküler yapıştırıcılar adı verilen protein parçalayıcıları geliştiriyor. PROTAC’lar gibi, proteinleri atmak için hücrenin enzimlerini – ubiquitin ligazlarını – kullanırlar. Ancak bir moleküler yapıştırıcı, ligaz ve proteini birbirine bağlamak yerine, yalnızca ligaza bağlanır ve enzimin yüzeyini değiştirir, böylece proteini bozunma için işe alır. Bu şekilde tasarlanmamış olsa da, multipl miyelom için en çok satan kanser ilaçlarından biri olan Revlimid moleküler bir tutkaldır.
Viyana’daki CeMM Moleküler Tıp Araştırma Merkezi’nde kimyasal biyolog ve KOODAC ekibinin bir üyesi olan Georg Winter, “Tutkal parçalayıcılarının en büyük avantajı, PROTAC’ların aksine, bozmak istediğiniz hedefe bağlanmanıza gerek olmamasıdır” diyor. Laboratuvarının rolü, KOODAC’ın hedef proteinlerini parçalayan moleküler yapıştırıcılar bulmaktır. Winter tarafından ortaklaşa kurulan Viyana’da bir biyoteknoloji firması olan Proxygen de dahil olmak üzere birçok şirket, PROTAC’lara daha küçük ve kimyasal olarak daha basit (bulması daha zor olsa da) alternatifler olabilecek moleküler tutkal bozurucuları arıyor.
Geçen yıla kadar Amgen’de araştırma başkanı olan Deshaies, protein bozunurlarının – PROTAC’ler ve moleküler yapıştırıcılar – büyük ölçekte başarılı olmasını bekliyor. Herhangi bir ilaç teknolojisini mükemmelleştirmenin, ilk ilaç piyasaya çıktıktan sonra bile zaman gerektirdiğini belirtiyor. “Oraya ulaşmak için endüstrinin on yıl boyunca kolektif çabası gerekiyor” diyor. “PROTAC’lar bu yörüngede hala erken.”
Mossé, birçok yeni tedavinin hastalarını hayal kırıklığına uğrattığını gördü, ancak PROTAC’ların farklı olacağını düşünüyor. “Sanırım çocuklara uyuşturucu götüreceğiz,” diyor. “Dizenin doğru olduğuna gerçekten ikna oldum.”
Lindberg benzer şekilde çocukluk çağı kanserlerine neden olan proteinleri ortadan kaldırmaya kararlıdır. Bu proteinler “oğlumu benden aldı”, diyor, “Onları diğer çocuklar için bir tehdit olarak çıkarmak istiyorum.”
Kaynak ve devamına Buradan ulaşabilirsiniz.
