Küçük hücreli olmayan akciğer kanserini tedavi etmek için devam eden mücadelenin ortasında, Stanford Üniversitesi bilim insanları tarafından yürütülen yeni bir çalışma, bir hastanın immünoterapiye tepkisinin, bağışıklık hücrelerinin tümörlerin etrafında nasıl kümelendiğine bağlı olabileceğini öne sürüyor. Sonuçları, tümörler içindeki belirli bağışıklık hücrelerinin mekansal düzenlemelerinin, mevcut biyobelirteç testlerini aşarak tedavi yanıtının güçlü belirleyicileri olarak hizmet edebileceğini ortaya koymaktadır.
Akciğer kanseri küresel kanser ölümlerine yol açar ve küçük hücreli olmayan varyantlar vakaların %80’inden fazlasını oluşturur. Bağışıklık kontrol noktası inhibitörleri tedaviyi dönüştürdü, ancak alıcıların yalnızca %27-45’ine yardımcı oldu.
İmmünoterapi yanıtı için güvenilir tahmin edici biyobelirteçler, şu anda PD-L1 immünohistokimyasına, tümör mutasyonel yüküne ve mikrouydu stabilite testlerine dayanan, her biri denemeler arasında mütevazı tahmin performansı sunan ve tutarsızlığa eğilimli olan klinisyenlerden kaçındı.
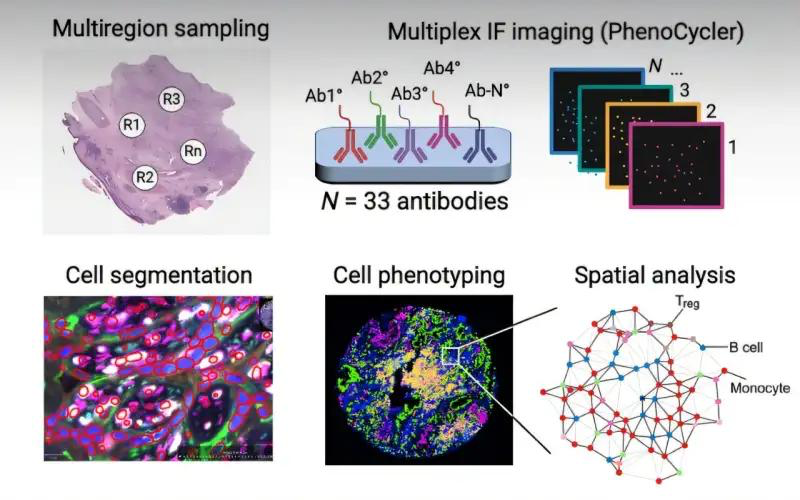
Science Advances’te yayınlanan “Tek hücreli çok modlu analiz, küçük hücreli olmayan akciğer kanserinde tedavi yanıtını öngören tümör mikroçevresini ortaya koyuyor” çalışmada, araştırmacılar, hasta sonuçlarıyla ilişkili tümör-bağışıklık mimarilerini belirlemek için çoklu immünofloresans, RNA dizilimi ve derin öğrenme odaklı histolojiyi birleştirdi.
Stanford Tıp Merkezi’nde tedavi edilen 132 küçük hücreli olmayan akciğer kanseri hastasından alınan doku örnekleri çalışmanın temelini oluşturdu. Bunlar arasında 50 hastaya yoğun multipleks immünofloresans (mIF) görüntülemesi tabilirken, 115 için tam slayt histoloji görüntüleri ve 122 için RNA dizileme verileri mevcuttu. Tüm modalitelerde 45 milyondan fazla hücre profillendi.
Çoklu immünofloresans, 255 doku çekirdeğinde 33 protein belirteci yakalayarak 1,5 milyon hücre için mekansal koordinatlar sağladı. Denetimsiz kümeleme, yerel mahalleleri sekiz fenotipte gruplandırdı. 2,2 milyon çekirdek üzerinde eğitilmiş ve 30 akciğer slaytında ince ayarlı NucSegAI adlı derin öğrenme modeli, 119 tam slayt histoloji görüntüsünde 45,6 milyon hücrenin haritasını çıkardı.
RNA-seq dekonvolüsyonu tahmin edilen bağışıklık hücresi fraksiyonları ve gen kümesi zenginleştirmesi, mekansal kalıpları sinyal yollarına bağladı. Bir sitotoksik T lenfosit (CTL) skoru, hasta başına sitotoksik T hücresi (Tc) ile zenginleştirilmiş mahallelerin fraksiyonunu özetledi.
Anti-PD-1/PD-L1 tedavisi alan 34 hasta arasında, yanıt vermeyenlere göre 2,5 kat daha fazla Tc hücresi ve 6,5 kat daha yüksek Tc zenginleştirilmiş mahalleler taşıdı. Bu tümörler ayrıca Tc ve dendritik hücreler (Dc), monositler ve tümör hücreleri arasında daha güçlü mekansal etkileşimler sergiledi.
CTL skor dağılımının üst yarısındaki hastalar önemli ölçüde daha uzun progresyonsuz sağkalımdan yararlanırken, makrofaj baskın mahalleler erken nüksetti.
Küçük hücreli olmayan akciğer kanseri olan eski sigara içenler, tümörlerinde daha sessiz bir bağışıklık ayak izi taşıma eğilimindeydi.
Stanford Üniversitesi’ndeki araştırmacılar, eski sigara içenlerden alınan tümör örneklerinin, bağışıklık hücrelerinin doğrudan kanser hücrelerine komşu olduğu önemli ölçüde daha az bölge içerdiğini buldular. Buna karşılık, hiç sigara içmeyenler, tümör hücrelerine bitişik daha yoğun lenfosit kümelerine sahipti.
Araştırmacılar, mekansal immünolojinin rutin patolojiyle entegre edilmesinin, pahalı bağışıklık kontrol noktası ilaçları için hasta seçimini keskinleştirebileceği ve diğerlerini toksik maruziyetten kurtarabileceği sonucuna varmıştır.
Daha geniş benimseme, standart H&E slaytlarından benzer içgörüler çıkaran ve hassas akciğer kanseri bakımına doğru akıcı bir yol vaat eden NucSegAI gibi yazılımlara bağlanabilir.
Kaynak ve devamına Buradan ulaşabilirsiniz.
