Araştırmacılar, 22q11.2 Silme Sendromu modellerinde hafızayı ve beyin hücresi fonksiyonunu geliştirmek için umut verici bir strateji belirlediler.
eLife’da yayınlanan çalışma, EMC10 proteininin seviyelerinin azaltılmasının 22q11.2 Deletion Sendromunun fare ve insan hücre modellerinde hem hücresel hem de bilişsel işlevi geri yükleyebileceğini göstermektedir. Editörler bunu, umut verici bir terapötik strateji olarak EMC10 indirgemesini destekleyen zorlayıcı kanıtlarla desteklenen önemli bir çalışma olarak tanımlıyor.
22q11.2 DiGeorge sendromu olarak da bilinen Deletion Syndrome, kromozom 22’deki küçük bir eksik genetik materyal bölümünün neden olduğu doğumdan itibaren mevcut olan genetik bir durumdur. Her 4.000 doğumdan yaklaşık 1’ini etkiler ve öğrenme gecikmeleri, konuşma güçlüğü, dikkat eksikliği bozuklukları ve yarık damak gibi çok çeşitli semptomlara yol açabilir. Aynı zamanda şizofreni gelişimi için bilinen en güçlü genetik risk faktörlerinden biridir. Bu durumu olan kişiler, semptomları ortaya çıktıkça izlemek ve yönetmek için genellikle ömür boyu bakıma ihtiyaç duyarlar.
Fare modellerinde, gen aktivitesini kontrol etmeye yardımcı olan mikroRNA adı verilen bir grup molekülün 22q11.2 Silme Sendromunda bozulduğu tespit edilmiştir. Bu bozulmanın önemli bir etkisi, membran proteinlerinin biyogenezinde rol oynayan Emc10 proteinini üreten bir gen olan Emc10’un aktivitesinde bir artıştır.
Emc10, bu membran proteinlerinin üretimine ve montajına yardımcı olarak, hücrelerin nasıl çalıştığı ve çevreleriyle nasıl etkileşime girdiği konusunda çok önemli bir rol oynar. (Not: Emc10 fare genini ifade ederken, büyük harfle yazılmış EMC10 eşdeğer insan genini ifade eder. Benzer şekilde, Emc10 farelerdeki proteini ifade ederken, EMC10 insanlardaki proteini ifade eder). Yazarlar daha önce Emc10 seviyelerinin azaltılmasının 22q11.2 Delesyon Sendromu fare modelinde belirli bilişsel semptomları tersine çevirebileceğini göstermişlerdir.
Mortimer B’de Yardımcı Araştırma Bilimcisi olan baş yazar Martin Lackinger, “Prevalansına ve ciddi etkisine rağmen, şu anda 22q11.2 Deletion Sendromunun altta yatan moleküler mekanizmalarını ele alan hedefli tedaviler yoktur” diyor. Zuckerman Zihin Beyin ve Davranış Enstitüsü, Columbia Üniversitesi, New York, ABD.
“Önceki bulgular üzerine inşa etmeyi ve EMC10 seviyelerinin durumun insan hücre modellerinde de artmadığını ve EMC10 aktivitesinin azaltılmasının semptomları hafifletip hafifletemeyeceğini test etmeyi amaçladık.”
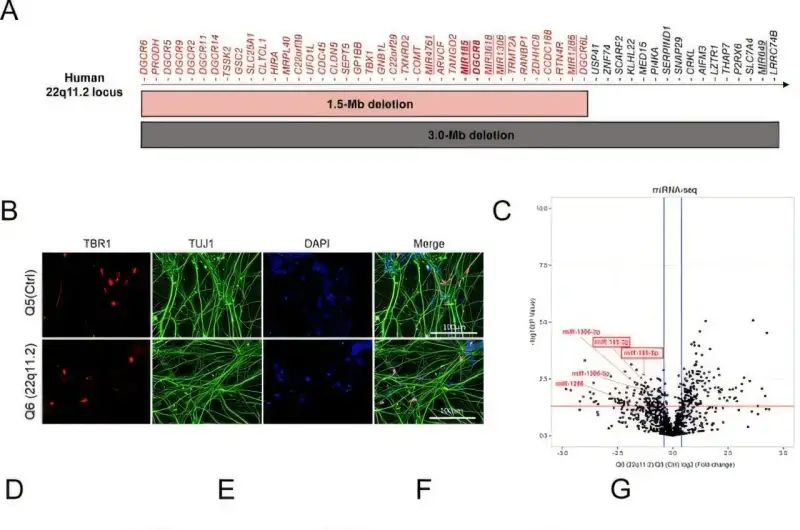
Bunu test etmek için ekip önce 22q11.2 Delesyon Sendromu olan ve olmayan kişilerden alınan kök hücrelerden nöronlar yarattı. Biri doğal gelişimi taklit eden ve diğeri hızlı bir şekilde nöron oluşturmak için NGN2 adı verilen bir gen kullanan iki yöntem kullanarak, 22q11.2 silinmesine sahip beyin hücrelerinin, beyin gelişiminde rol oynayan miR-185 de dahil olmak üzere belirli mikroRNA seviyelerini düşürdüğünü buldular. Beklendiği gibi, mikroRNA aktivitesindeki bu düşüş aynı zamanda anormal derecede yüksek EMC10 seviyelerine de yol açtı.
22q11.2 Deletion Syndrome’un fare modelleri, diğer nöronlardan sinyal alan bir sinir hücresinin kısa, dallı uzantısı olan beyin dendritlerinin bozulmuş oluşumunu göstermektedir – Emc10 seviyelerinin azalmasıyla kısmen tersine çevrilen bir sorun. Araştırmacılar, aynı şeyin insan nöronlarında da gerçekleşip gerçekleşmediğini test etmek için 22q11.2 silme nöronlarındaki EMC10 seviyelerini azaltmak için genetik düzenleme araçlarını kullandılar.
22q11.2 Delesyon Sendromu olan kişilerden tedavi edilmeyen nöronlarda dendritler daha kısa, daha az ve daha az karmaşıktı. Ancak EMC10 azaltıldığında, dendritik büyüme normal seviyelere geri döndü. İlginç bir şekilde, tam EMC10 çıkarılmış nöronlar, kontrol nöronlarından daha fazla dallanma gösterdi ve bu da güçlü bir restoratif etki olduğunu düşündürdü.
Ekip ayrıca nöronların beyindeki önemli bir haberci olan kalsiyumu kullanarak ne kadar iyi sinyal verebileceğini ölçtü. Yüksek EMC10’a sahip 22q11.2 silme hücrelerinde kalsiyum sinyalizasyonu zayıftı. Ancak EMC10’u azalttıktan sonra, hücrelerin kalsiyum tepkisi normale döndü.
EMC10’un daha geniş etkisini anlamaya çalışan araştırmacılar, hangi genlerin açık veya kapalı olduğuna bakmak için transkriptomik profilleme kullandılar. EMC10’un azaltılması, beyin gelişimi, sinaps oluşumu ve hücre sinyalizasyonunda yer alanlar da dahil olmak üzere yüzlerce genin aktivitesini geri kazandırdı.
RBFOX1, RGS4 ve PCDHA2 gibi düzeltilmiş genlerin birçoğunun şizofreni riski ile ilişkili olduğu zaten bilinmektedir ve bu da 22q11.2 Deletion Sendromunda görülen psikiyatrik semptomları potansiyel olarak açıklar.
Bu hücresel bulguların gerçek dünyadaki bir tedaviye dönüşüp dönüşemeyeceğini test etmek için ekip daha sonra yetişkin fare modellerine odaklandı. Yüksek EMC10 seviyelerinin olgun beyinde devam eden sorunlara neden olup olmayacağını veya erken gelişim sırasında beyin olgunlaşması üzerinde geri dönüşü olmayan bir etkiye neden olup olmadığını belirlemeyi amaçladılar.
Bu amaçla, yetişkin farelerde Emc10 seviyelerini 22q11.2 silme ile düşürdüler ve sosyal bellek testlerinde ne kadar iyi performans gösterdiklerini karşılaştırdılar. Bu, şizofreni ve 22q11.2 Delesyon Sendromunda sıklıkla bozulan işlevler olan başkalarını tanımayı ve geçmiş sosyal deneyimleri hatırlamayı içeren temel bir bilişsel beceridir.
Tedavi edilen fareler, tedavi edilmeyen farelerden önemli ölçüde daha iyi performans gösterdi ve aktivite seviyeleri, kaygıları ve genel davranışları değişmeden kaldı. Bu, 22q11.2 silme ile yetişkin farelerde Emc10 seviyelerinin geri yüklenmesinin bilişsel eksiklikleri önemli ölçüde iyileştirebileceğini, terapötik müdahale için geniş bir pencereyi vurgulayabileceğini ve Emc10’u doğum sonrası müdahaleler için umut verici bir hedef olarak belirleyebileceğini göstermektedir.
Potansiyel bir tedavi stratejisini araştırmak için araştırmacılar, Emc10’un diğer nöronlarla iletişimini engellemek için tasarlanmış kısa sentetik genetik malzeme iplikleri olan antisense oligonükleotidler (ASO’lar) yarattılar. Bu ASO’lar sekiz haftalık yetişkin farelerin beynini çevreleyen sıvıya (beyin omurilik sıvısı) uygulandı ve hipokampus ve prefrontal korteks gibi önemli bölgelerde Emc10 seviyelerini başarıyla azalttı. Ekip ayrıca hem sosyal hem de mekansal hafızayı geliştirdiklerini buldu.
Emc10 geninin farklı bir bölgesini hedefleyen ikinci bir ASO, aynı etkileri üreterek bu sonucu doğruladı. Önemli olarak, faydalar her iki ASO ile de sürdü. Fareler, tek bir ASO tedavisinden sonra iki aydan fazla bir süre boyunca gelişmiş hafıza gösterdi. Emc10 seviyeleri, dokuz haftalık işarette birden fazla beyin bölgesinde düşük kaldı. Bu, tedavinin etkilerinin uzun süreli olduğunu ve seyrek dozlama ile potansiyel olarak yönetilebilir olduğunu göstermektedir.
Mortimer B Baş Araştırmacısı kıdemli yazar Joseph Gogos, “Bulgularımız, EMC10 seviyelerini düşüren tedavilerin 22q11.2 Deletion Syndrome’da görülen bazı temel bilişsel semptomları tersine çevirmenin bir yolu olabileceğine dair güçlü klinik öncesi kanıtlar gösteriyor” diyor. Zuckerman Zihin Beyin ve Davranış Enstitüsü ve Stavros Niarchos Vakfı (SNF) Hassas Psikiyatri ve Ruh Sağlığı Merkezi’nin eş direktörü, Columbia Üniversitesi.
“Özellikle umut verici olan, farelerde gördüğümüz gelişmelerin yetişkinlikte gerçekleşebileceği ve 22q11.2 silme ile ilişkili bilişsel ve davranışsal semptomlarda terapötik ve önleyici müdahale için geniş bir zamansal pencereyi vurgulayarak kalıcı olmalarıdır.
“Gelecekteki çalışmaların, tedavinin potansiyel olarak kliniğe getirilebilmesi için uzun vadeli güvenliği, optimum dozlamayı ve EMC10 hedefli tedavilerin bozukluğun diğer özellikleriyle nasıl etkileşime girdiğini araştırması gerekecektir.”
Kaynak ve devamına Buradan ulaşabilirsiniz.
