Melbourne’lü bilim insanları, “Hippo yolu”nun moleküler düzeyde nasıl çalıştığını ortaya çıkararak, bu yolun nasıl kontrol sağladığı ve ölümcül kanser türü mezotelyoma için çok ihtiyaç duyulan bir tedavi olarak potansiyeli konusunda anlayışı geliştiriyor.
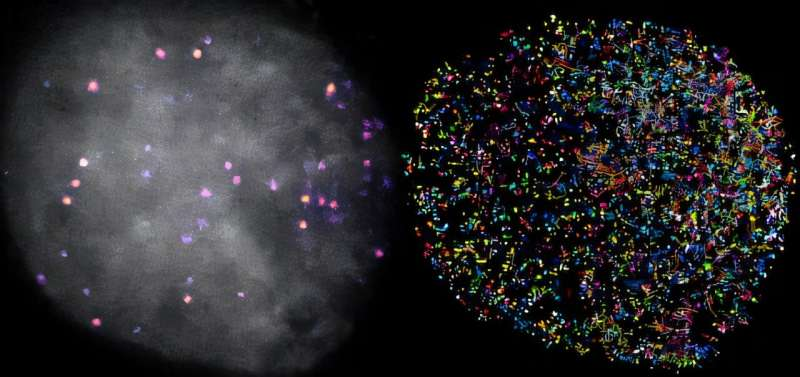
Hippo yolunun nasıl çalıştığına dair önemli bir rol oynayan TEAD ve YAP adı verilen bir grup DNA bağlayıcı proteinin aktivitesini gösteren mikroskopik görüntüyü ilk kez filme aldılar.
Profesör Kieran Harvey, Hippo yolunun canlılarda bir milyar yıldan fazla bir süre önce ortaya çıktığını ve bugün tek hücreli organizmalardan memelilere, hatta insanlara kadar çeşitli türlerde aynı şekilde çalıştığını açıklıyor.
Sağlıklı doku ve organların nasıl büyüdüğünü, yaraların nasıl iyileştiğini, hücrelerin nasıl çoğaldığını ve gerektiğinde nasıl öldüğünü kontrol eder ve Hippo yolu ayrıca kanser geliştiğinde ve vücutta yerleştiğinde de rol oynar.
Hippo yolu üzerinde etkili olan iki yeni ilaç, şu anda Peter Mac’te ilk insan deneylerinde yer alıyor ve bunları, genellikle asbeste maruz kalmanın neden olduğu, tedavisi zor bir kanser türü olan mezotelyoma için potansiyel tedaviler olarak değerlendiriyor.
Peter Mac ve Monash Üniversitesi’nde çifte görev yapan Profesör Harvey, “Su aygırı yolu, vücudun DNA’mızdan gelen talimatları nasıl yerine getirdiğini kontrol eden transkripsiyonu kontrol ediyor ancak bunu nasıl yaptığı tam olarak anlaşılamıyor” diyor.
“Bu çalışmada, bu sinyal yolunda yer alan proteinlerin insan hücrelerinin çekirdeğinde hareket ederek DNA’ya nasıl bağlandığını gerçek zamanlı olarak ilk kez kaydetmemizi sağlayan yeni mikroskopi tekniklerini kullandık.
“Bu proteinlerin farklı zaman ölçeklerinde DNA ile nasıl etkileşime girdiğini inceledik ve önemli bir bulgu, Hippo yolunun, TEAD’lerin ve YAP’ın DNA’ya bağlanma süresini kontrol ederek hücreler tarafından hangi genlerin üretileceğini belirlemesidir.”
Özellikle TEAD1’in (TEAD’lerden biri) mezotelyoma gelişiminde ve ilerlemesinde rol oynadığı bilinmekte olup, TEAD’leri inhibe eden ilaçlar terapötik fayda beklentisiyle değerlendirilmektedir.
Nadir görülen bir diğer kanser epiteloid hemanjioendotelyoma türü ise füzyon proteini YAP-TFE3’ten kaynaklanır ve bu çalışma, YAP’ın bu mutasyona uğramış versiyonunun DNA’ya YAP veya TEAD’lerden daha uzun zaman dilimlerinde bağlandığını da göstermiştir.
Peter Mac ve Monash Üniversitesi’nden Dr. Benjamin Kroeger liderliğindeki araştırma, bu proteinlerin yeni kanser ilaçları tarafından nasıl hedef alınabileceğinin anlaşılmasında önemli sonuçlar doğuruyor. Makale, Science Advances dergisinde yayımlandı .
Kaynak ve devamına Buradan ulaşabilirsin.
