Broad Institute araştırmacıları, Huntington hastalığının ve Friedreich ataksisinin kökündeki genetik dizileri düzenlemenin bir yolunu geliştirdiler.
Koşullar, arka arkaya tekrarlanan üç harfli DNA uzantılarının neden olduğu 40’tan fazla ciddi nörolojik bozukluktan ikisidir. Belirli bir eşik uzunluğundan daha uzunsa, bu diziler kontrolsüz bir şekilde uzar ve Huntington hastalığında beyin hücresi ölümüne ve Friedreich ataksisinde sinir liflerinin parçalanmasına yol açar. Bu hastalıkların ilerlemesini durduran hiçbir tedavi yoktur.
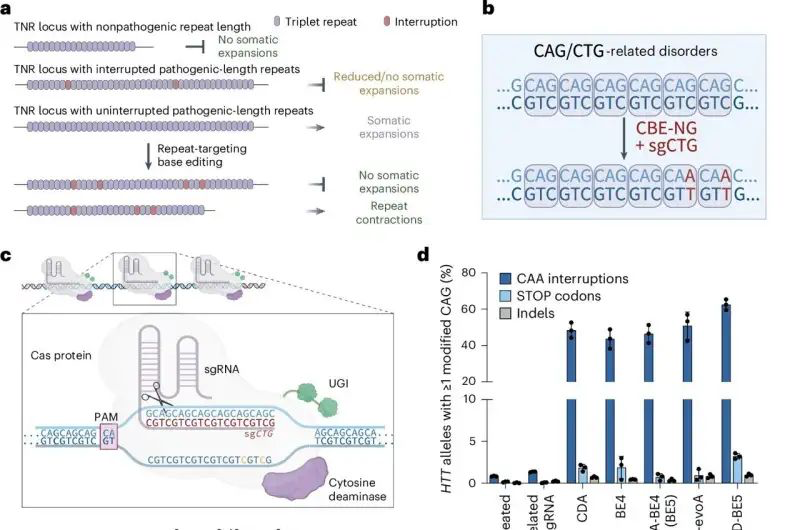
Broad ekibi, bu DNA tekrarlarının genişlemesini önlemek için yeni bir yaklaşım geliştirdi. Temel düzenleme adı verilen bir tekniği kullanan ekip, DNA’nın tekrarlanan geriliminin ortasına tek harfli değişiklikler getirdi ve Huntington hastalığı ve Friedreich ataksisinin hasta hücrelerinde ve fare modellerindeki diziyi kesintiye uğrattı. Düzenlenmiş DNA yollarının uzunluk olarak aynı kaldığını ve hatta zamanla kısaldığını buldular.
Bulgular yakın zamanda Nature Genetics’te yayınlandı ve Richard Merkin Profesörü ve Broad’deki Merkin Sağlık Hizmetlerinde Dönüştürücü Teknolojiler Enstitüsü direktörü olan gen düzenleme öncüsü David Liu’nun laboratuvarından geldi. Liu aynı zamanda Broad’de Friedreich’s Ataxia Accelerator’da araştırmacı, Harvard Üniversitesi’nde profesör ve Howard Hughes Tıp Enstitüsü araştırmacısıdır.
Çalışma başladığında Liu’nun laboratuvarında doktora sonrası araştırmacı olan ve şu anda Boston Çocuk Hastanesi’nde yardımcı doçent olarak Lodish Ailesi kürsüsünde bulunan Mandana Arbab ve o zamanlar yüksek lisans öğrencisi olan Zaneta Matuszek, çalışmanın ortak ilk yazarlarıdır. Broad ilişkili bir bilim adamı ve Mass General Research Institute’da yardımcı doçent olan Ricardo Mouro Pinto, Liu ile birlikte ortak bir yazardır.
Bu düzenlemelerin genoma yerleştirilmesinin potansiyel yan etkilerini kataloglamak için daha fazla çalışmaya ihtiyaç duyulacak, ancak araştırmacılar yaklaşımın bu tür DNA tekrarlarının neden olduğu hastalıkları anlamak için değerli bir araç olabileceğini söylüyor.
Liu, “Bu tekrarları bir temel editörle bozmanın hastaları tedavi etmek için uygulanabilir bir terapötik strateji olup olamayacağını bilmeden önce çok daha fazla çalışmaya ihtiyaç duyulacaktır” dedi. “Ancak kesintiye uğrayan tekrarların biyolojik sonuçlarını aydınlatabilmek gerçekten yararlı ve önemli bir dönüm noktasıdır.”
Tekrar kesintiye uğradı
Yaklaşık 3.000 kişiden birinde DNA’daki üç harfli tekrarların neden olduğu bir hastalık vardır. Aynı hastalığa sahip bireyler farklı sayıda DNA tekrarını miras alabilir – daha fazla tekrarı olan kişiler genellikle semptomları daha erken ve daha şiddetli yaşarlar ve hastalıkları daha hızlı ilerler.
Buna karşılık, bazı hastalar bu tekrarlarda doğal olarak meydana gelen tek harfli “kesintilere” sahiptir ve daha sonra gelişen daha hafif semptomlara sahiptir. Bu bireylerin hastalıklarını çocuklarına geçirme olasılıkları da kesintisiz tekrarları olan insanlara göre daha düşüktür.
Bu, Matuszek ve Arbab’a bir fikir verdi. Bir gen düzenleme terapisi, bazı hastalarda doğal olarak meydana gelenleri taklit eden bir kesinti sağlayabilirse, tekrarın genişlemesini durdurabilir ve hastalığın ilerlemesini durdurabilir veya yavaşlatabilir.
Matuszek ve Arbab, DNA’da tek harfli değişiklikler yapmak için 2016 yılında Liu’nun laboratuvarı tarafından geliştirilen bir araç olan temel düzenlemeyi kullanmaya karar verdiler. Huntington hastalığı için bir CAG tekrar sistemi içinde bazı G•C çiftlerini A•T çiftlerine değiştiren bir sistem buldular. Bir diğeri, Friedreich’in ataksisinin GAA tekrarları içinde G•C çiftlerine birkaç A•T çiftini düzenledi.
Ekip, editörleri bozukluğu olan hastalardan elde edilen bağ dokusu hücrelerinde test ettiğinde, tedavi edilen hücrelerdeki tekrarların sayısı zaman içinde aynı kaldı veya hatta azaldı – ancak tedavi edilmeyen hücreler eskisinden daha fazla tekrar yaptı.
Temel editörleri farelerdeki belirli hücrelere mekeklemek için araştırmacılar, onları nöronlara kargo iletmek için tasarlanmış adeno ile ilişkili bir virüs olan çift AAV9 vektörlerine paketlediler. Temel editörler, Friedreich ataksisi ve Huntington hastalığının fare modellerinde tekrar yollarını stabilize etti.
Matuszek, “Gerçekten heyecan verici olan şey, artık hücre ve hayvan modellerinde kesintiler tanıtmak ve bu hastalıkların biyolojisini nasıl etkilediklerini incelemek için bir araca sahip olmamızdır” dedi.
Yeni bir düzenleme stratejisi
Liu, bu tekrar dizilerinin genomun başka yerlerinde gerçekleştiğinden, temel editörlerin genomun bu kısımlarında düzenlemeler yapabileceği ve istenmeyen yan etki olasılığını artırabileceği konusunda uyarıyor.
Ancak şimdiye kadar ekibi, hedef dışı düzenlemenin çoğunun genomun genler arasında bulunan veya proteinleri kodlamayan kısımlarında meydana geldiğini ve insanlarda istenmeyen yan etki olasılığını azalttığını buldu. Araştırmacılar, bu etkileri insan hastalığını daha sadık bir şekilde yansıtan belirli hücre popülasyonlarında ve hayvan modellerinde incelemeyi planlıyorlar.
Bununla birlikte, ekip, tekrarlayan yollarda kesintiler getiren terapötik bir stratejinin bir gün Huntington, Friedreich ataksisi ve diğer trinükleotid tekrar bozukluklarının tedavisine yardımcı olabileceğini düşünüyor, çünkü DNA’daki bu tür değişiklikler, hastalığı olmayan veya yalnızca hafif semptomları olan kişilerde doğal olarak meydana geliyor.
Arbab, “Bu çalışma sadece ilk kez kesintilere neden olmanın tekrarlar üzerinde derin bir dengeleyici etkiye sahip olduğunu göstermekle kalmıyor, aynı zamanda kullandığımız temel düzenleme yaklaşımının bir düzineden fazla tekrar bozukluğundan herhangi birini incelemek için de uygulanabileceğini” dedi. “Hala yapılacak çok iş var, ancak bu yaklaşımın bu hastalıkların çoğu için terapötik gelişimi gerçekten hızlandırabileceğinden umutluyuz.”
Bu arada, araştırmacılar, hastalığa neden olan tekrarlayan yolları aynı anda daha kısa, kararlı sayıda tekrarla değiştirmek için asal düzenlemeyi kullanarak farklı bir yaklaşım da geliştiriyorlar.
Kaynak ve devamına Buradan ulaşabilirsiniz.
