Genomik ve laboratuvar çalışmaları, Reelin’in nöronal kırılganlık karşısındaki kilit rolü ve bilişi sürdürmede kolin ve antioksidanların rolü de dahil olmak üzere çok sayıda bulguyu ortaya koyuyor.
Nature dergisinde bugün yayımlanan , MIT tarafından yapılan ve erişime açık bir araştırma, Alzheimer hastalığında belirli hücrelerin ve devrelerin nasıl savunmasız hale geldiğine dair yeni kanıtlar sunuyor ve bazı kişilerin, hastalık patolojisinin açık belirtilerine rağmen bilişsel gerilemeye karşı dayanıklılık göstermesine yardımcı olabilecek diğer faktörlere odaklanıyor.
Bilişsel işlevleri ve hafızayı sürdürmeye yönelik müdahaleler için potansiyel hedefleri vurgulamak amacıyla yazarlar, Alzheimer hastalığı olan ve olmayan kişilerde birden fazla beyin bölgesindeki gen ifadesinin yeni bir karşılaştırmasını yaptılar ve önemli bulgularını test etmek ve doğrulamak için laboratuvar deneyleri yürüttüler.
Beyin hücrelerinin hepsinin DNA’sı aynıdır ancak onları hem kimlikleri hem de aktiviteleri açısından farklı kılan şey, bu genleri nasıl ifade ettiklerine dair kalıplarıdır. Yeni analiz, 48 doku donöründen altı beyin bölgesindeki 70’ten fazla hücre tipinde 1,3 milyondan fazla hücrede gen ifadesi farklılıklarını ölçtü; bunlardan 26’sı Alzheimer teşhisiyle ve 22’si ise teşhisi olmadan öldü. Bu nedenle çalışma, Alzheimer hastalığı sırasında beyin hücresi aktivitesinin hücre tipine, beyin bölgesine, hastalık patolojisine ve her bir kişinin hayattayken bilişsel değerlendirmesine göre nasıl farklılık gösterdiğine dair benzersiz derecede büyük, kapsamlı ve yine de ayrıntılı bir muhasebe sağlıyor.
“Belirli beyin bölgeleri Alzheimer’da savunmasızdır ve bu bölgelerin veya belirli hücre tiplerinin nasıl savunmasız olduğunu anlamak için önemli bir ihtiyaç vardır,” diyor ortak kıdemli yazarlardan Li-Huei Tsai , Picower Nörobilim Profesörü ve MIT’deki Picower Öğrenme ve Bellek Enstitüsü ve Yaşlanan Beyin Girişimi direktörü . “Ve beyin sadece nöronlardan ibaret değildir. Birçok başka hücre tipi vardır. Bu hücre tiplerinin nerede olduklarına bağlı olarak nasıl farklı tepki verebilecekleri, henüz incelemeye başladığımız büyüleyici bir konudur.”
Bilgisayar bilimi profesörü ve MIT Hesaplamalı Biyoloji Grubu başkanı olan kıdemli ortak yazar Manolis Kellis , gen ifadesi karşılaştırmalarını ölçmek için kullanılan tekniği, yani tek hücreli RNA profillemesini, bir asırdan fazla bir süre önce Alois Alzheimer’ın hastalığın patolojisini karakterize etmesini sağlayan mikroskoplardan çok daha gelişmiş bir “mikroskop” olarak nitelendiriyor.
Kellis, “Alzheimer mikroskobunda amiloid protein plakları ve fosforlanmış tau düğümleri görürken, bizim tek hücreli ‘mikroskopumuz’ bize patolojiye yanıt olarak hücre hücre ve gen gen binlerce ince ama önemli biyolojik değişim hakkında bilgi veriyor,” diyor. “Bu bilgileri hastaların bilişsel durumuyla ilişkilendirmek, hücresel yanıtların bilişsel kayıp veya dayanıklılıkla nasıl ilişkili olduğunu ortaya koyuyor ve bilişsel kaybı tedavi etmek için yeni yollar önermeye yardımcı olabilir. Patoloji, bilişsel gerileme teşhis edilmeden önce bilişsel semptomlardan bir veya iki on yıl önce ortaya çıkabilir. Bu aşamada patoloji hakkında yapabileceğimiz fazla bir şey yoksa, en azından bilişsel işlevi koruyan hücresel yolları korumaya çalışabiliriz.”
Tsai Laboratuvarı’nda eski bir MIT doktora sonrası araştırmacısı olan ve şu anda Pittsburgh Üniversitesi’nde yardımcı doçent olan Hansruedi Mathys; Kellis’in laboratuvarında eski bir lisansüstü öğrencisi olan ve şu anda Harvard Tıp Fakültesi’nde doktora sonrası araştırmacı olan Carles Boix PhD ’22; ve Tsai’nin laboratuvarında lisansüstü öğrencisi olan Leyla Akay, prefrontal korteks, entorinal korteks, hipokampüs, anterior talamus, angular girus ve orta temporal korteksi analiz eden çalışmaya öncülük etti. Beyin örnekleri Rush Üniversitesi’ndeki Dini Tarikat Çalışması ve Rush Hafıza ve Yaşlanma Projesi’nden geldi.
Sinirsel kırılganlık ve Reelin
Alzheimer’daki amiloid patolojisinin ve nöron kaybının en erken belirtilerinden bazıları, hipokampüs ve entorinal korteks adı verilen hafıza odaklı bölgelerde görülür. Araştırmacılar, bu bölgelerde ve serebral korteksin diğer kısımlarında olası bir nedeni saptayabildiler. Hipokampüsteki bir tür uyarıcı nöron ve entorinal korteksteki dört nöron, Alzheimer’lı kişilerde olmayan kişilere göre önemli ölçüde daha azdı. Bu hücrelerde azalma olan kişiler bilişsel değerlendirmelerde önemli ölçüde daha kötü performans gösterdi. Dahası, birçok savunmasız nöron ortak bir nöronal devrede birbirine bağlıydı. Ve en önemlisi, birçoğu doğrudan Reelin adı verilen bir proteini ifade ediyordu veya Reelin sinyallemesinden doğrudan etkilenmişti. Dolayısıyla, bulgular genel olarak, kaybı bilişsel yeteneklerin azalmasıyla ilişkili olan, nöronal bir devreyi ve moleküler bir yolu paylaşan özellikle savunmasız nöronları belirgin şekilde vurguluyor.
Tsai, Reelin’in Kolombiya’daki bir adam üzerinde yapılan son bir çalışma nedeniyle Alzheimer araştırmalarında öne çıktığını belirtiyor . Reelin geninde proteinin daha aktif olmasına neden olan nadir bir mutasyon vardı ve erken başlangıçlı Alzheimer’a karşı güçlü bir aile yatkınlığına sahip olmasına rağmen ileri yaşta bilişsel olarak sağlıklı kalabilmişti. Yeni çalışma, Reelin üreten nöronların kaybının bilişsel gerilemeyle ilişkili olduğunu gösteriyor. Hepsi bir arada ele alındığında, beynin Reelin’den faydalandığı, ancak onu üreten nöronların en azından bazı Alzheimer hastalarında kaybolabileceği anlamına gelebilir.
Akay, “Reelin’in belki bir tür koruyucu veya faydalı etkiye sahip olduğunu düşünebiliriz” diyor. “Ancak ne işe yaradığını veya dayanıklılığı nasıl sağlayabileceğini henüz bilmiyoruz.”
Araştırmacılar daha detaylı analizlerde, daha önce bu gruptan yapılan bir çalışmada tanımlanan prefrontal korteksteki özellikle hassas inhibitör nöron alt tiplerinin de Reelin sinyallemesinde rol oynadığını buldular ve bu durum molekülün ve sinyal yolunun önemini daha da güçlendirdi.
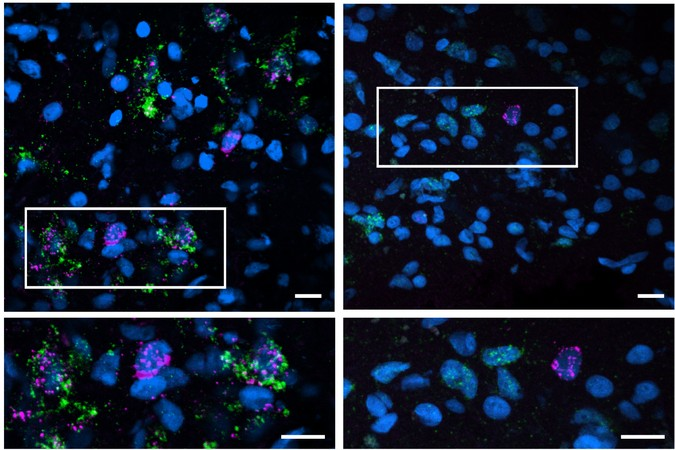
Sonuçlarını daha fazla kontrol etmek için ekip, doğrudan insan beyin dokusu örneklerini ve iki tür Alzheimer model faresinin beyinlerini inceledi. Gerçekten de, bu deneyler insan ve fare entorinal korteksindeki Reelin pozitif nöronlarda bir azalma gösterdi.
Astrositlerde kolin metabolizmasıyla ilişkili dayanıklılık
Bilişi patolojiye rağmen koruyabilecek faktörleri bulmak için ekip, hangi genlerin, hangi hücrelerde ve hangi bölgelerde, gözlemlenen patoloji göz önüne alındığında beklenen tipik bilişsel kaybın üzerinde, kalıntı bilişsel işlev olarak tanımladıkları bilişsel dayanıklılıkla en yakından ilişkili olduğunu inceledi.
Analizleri şaşırtıcı ve belirli bir yanıt verdi: Birkaç beyin bölgesinde, antioksidan aktivite ve kolin metabolizması ve poliamin biyosentezi ile ilişkili genleri ifade eden astrositler, yüksek tau ve amiloid seviyelerine rağmen, sürdürülebilir bilişle önemli ölçüde ilişkiliydi. Sonuçlar, Tsai ve Susan Lundqvist tarafından yönetilen ve kolin diyet takviyesinin astrositlerin en önemli Alzheimer risk geni olan APOE4 varyantının neden olduğu lipit düzensizliğiyle başa çıkmasına yardımcı olduğunu gösteren önceki araştırma bulgularını destekledi. Antioksidan bulguları ayrıca, anti-inflamatuar özelliklere sahip olabilecek bir diyet takviyesi olarak bulunabilen spermidin adlı bir moleküle işaret etti, ancak böyle bir ilişkinin nedensel olarak kurulması için daha fazla çalışmaya ihtiyaç vardır.
Daha önce olduğu gibi, ekip tek hücreli RNA ifade analizinden elde edilen tahminlerin ötesine geçerek örneklerin beyin dokusunda doğrudan gözlemler yaptı. Bilişsel olarak dayanıklı bireylerden gelenler, bilişsel dayanıklılıkla ilişkili olduğu tahmin edilen astrosit ifadeli genlerin birkaçının ifadesinde artış gösterdi.
Yeni analiz yöntemi, açık veri seti
Tek hücreli verilerin dağlarını analiz etmek için araştırmacılar, koordineli olarak ifade edilen gen gruplarına (gen modülleri olarak bilinir) dayanan yeni ve sağlam bir metodoloji geliştirdiler; böylece aynı modüldeki işlevsel olarak ilişkili genler arasındaki ifade korelasyon modellerinden yararlandılar.
Kellis, “Prensipte, incelediğimiz 1,3 milyon hücre, 20.000 genini astronomik sayıda farklı kombinasyonda kullanabilirdi,” diye açıklıyor. “Ancak pratikte, koordineli değişikliklerin çok daha küçük bir alt kümesini gözlemliyoruz. Bu koordineli kalıpları tanımak, çok daha sağlam değişiklikler çıkarsamamızı sağlıyor, çünkü bunlar aynı işlevsel olarak bağlı modüldeki birden fazla gene dayanıyor.”
Şu benzetmeyi sundu: Vücutlarında birçok eklem bulunan insanlar her türlü çılgınca şekilde hareket edebilirler, ancak pratikte yürüme, koşma veya dans etme gibi çok daha az koordineli hareketler yaparlar. Yeni yöntem, bilim insanlarının bu tür koordineli gen ifadesi programlarını bir grup olarak tanımlamasını sağlar.
Kellis ve Tsai’nin laboratuvarları veri setinden birkaç kayda değer bulguyu bildirmiş olsa da araştırmacılar, veri hazinesinde daha birçok olası önemli keşfin bulunmayı beklediğini düşünüyor. Bu tür keşifleri kolaylaştırmak için ekip, Kellis’in web sitesinde verilerle birlikte kullanışlı analitik ve görselleştirme araçları yayınladı .
“Veri seti inanılmaz derecede zengin. Sadece çok, çok ilginç olduğuna inandığımız birkaç önemli noktaya odaklandık, ancak bu veri setiyle öğrenilebilecek şeyleri kesinlikle tüketmedik,” diyor Kellis. “Önümüzde çok daha fazla keşif bekliyoruz ve genç araştırmacıların (her yaştan) hemen konuya dalıp bizi çok daha fazla içgörüyle şaşırtmasını umuyoruz.”
Kellis, araştırmacıların ileride farklı şekilde ifade edilen genlerle ilişkili kontrol devrelerini inceleyerek, beyin bölgeleri, hücre tipleri ve hastalığın farklı evreleri boyunca hastalık devrelerini tersine çevirmek için modüle edilebilen genetik varyantları, düzenleyicileri ve diğer sürücü faktörleri anlamaya çalıştıklarını söylüyor.
Araştırmanın diğer yazarları arasında Ziting Xia, Jose Davila Velderrain, Ayesha P. Ng, Xueqiao Jiang, Ghada Abdelhady, Kyriaki Galani, Julio Mantero, Neil Band, Benjamin T. James, Sudhagar Babu, Fabiola Galiana-Melendez, Kate Louderback, Dmitry yer alıyor. Prokopenko, Rudolph E. Tanzi ve David A. Bennett.
Araştırmaya destek verenler arasında Ulusal Sağlık Enstitüleri, Picower Öğrenme ve Hafıza Enstitüsü, JPB Vakfı, Cure Alzheimer’s Fund, Robert A. ve Renee E. Belfer Aile Vakfı, Eduardo Eurnekian ve Joseph DiSabato yer alıyor.
Kaynak …
