Çoğu insanda, solunum sinsitiyal virüsü (RSV) ve insan metapnömovirüsü (hMPV) olarak bilinen akciğeri enfekte eden patojenler hafif soğuk algınlığı benzeri semptomları tetikler. Ancak bebeklerde ve yaşlılarda bu virüsler şiddetli zatürreye ve hatta ölüme neden olabilir.
Ancak her iki virüse karşı aşı tasarlamak zordu. Şimdi, Scripps Research bilim insanları, onu hedef alan aşıları daha iyi tasarlamak için kritik bir RSV ve hMPV proteininin yapısını ve stabilitesini analiz ettiler. Nature Communications’da yayınlanan araştırmaları , mevcut olanlardan daha etkili olabilecek RSV aşılarının yanı sıra ticari olarak mevcut bir seçeneği olmayan hMPV’ye karşı bir aşıya işaret ediyor.
“Bu virüsler için bir karma aşı oluşturmak, hem bebekler hem de yaşlılar için viral hastane yatışlarını önemli ölçüde azaltabilir,” diyor çalışmanın kıdemli yazarı, Scripps Research’teki Bütünleşik Yapısal ve Hesaplamalı Biyoloji Bölümü’nde doçent olan Jiang Zhu, Ph.D.. “Bu, aynı zamanda çoğu RSV ve hMPV vakasının görüldüğü grip mevsiminde genel sağlık yükünü hafifletebilir.”
Bilim insanları uzun zamandır bağışıklık sistemini RSV, hMPV ve ilgili virüslerin yüzeylerinde bulunan füzyon (F) proteinlerini tanımaya ikna eden aşılar yaratmaya çalışıyorlar. Bu proteinler virüslerin insan hücrelerini enfekte etmesinde önemli bir rol oynuyor. Ancak F proteini, virüsler hücrelerle füzyon yaptığında “füzyon öncesi” formdan “füzyon sonrası” forma hızla değişen hassas bir yapıya sahip. İdeal olarak, bir aşı bağışıklık sistemine enfeksiyonu durdurabilmesi için kapalı füzyon öncesi F proteinini tanımayı öğretecektir.
Zhu, “Sorun şu ki bu füzyon öncesi yapı çok kırılgan ve değişken,” diyor. “Çevreyi birazcık bile değiştirirseniz, protein aniden bir arabadan bir robota dönüşen bir transformatöre benziyor.”
Bu, bilim insanlarının izole edilmiş bir füzyon öncesi F proteinini aşı olarak kullanamayacakları anlamına gelir; yapısı bağışıklık sisteminin tepki vermesi için çok hızlı değişir. Ve proteinin füzyon sonrası versiyonunu hedef alan bir aşı, bağışıklık sistemine virüse vücudu enfekte etme şansı olmadan saldırmayı öğretemez.
Biyofizik alanında geçmişi olan ve yakın zamanda HIV, SARS-CoV-2 ve hepatit C gibi virüslere karşı yeni aşılar tasarlayan Zhu, füzyon öncesi F proteininin neden bu kadar kararsız olduğunu, özellikle de neden açılmasının bu kadar kolay olduğunu tam olarak anlayabilirse daha kararlı bir form ve dolayısıyla daha iyi bir aşı üretebileceğini düşündü.
Zhu ve araştırma ekibi, öncelikle piyasada bulunan Arexvy, mResvia ve Abrysvo adlı dört mevcut RSV aşısının ve 3. faz denemelerine ulaşan deneysel bir aşının geliştirilmesinde kullanılan F proteinlerini analiz etti.
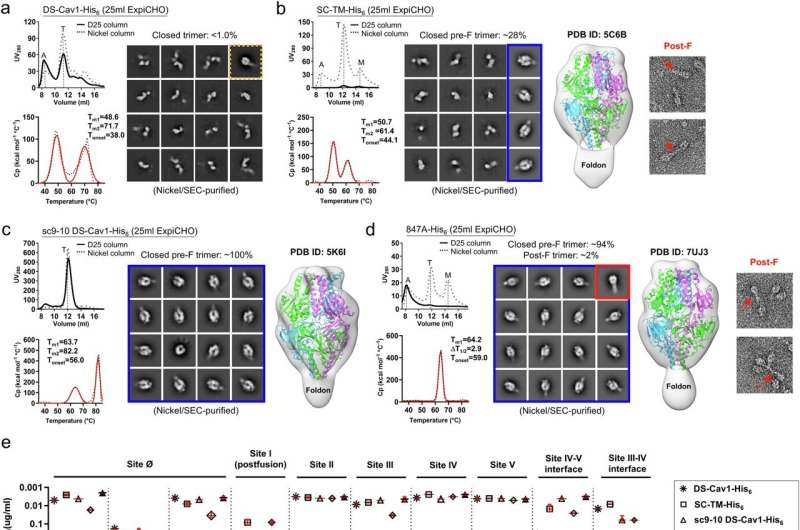
Bazı füzyon öncesi F proteinlerinin dengesiz göründüğünü ve bazen açık bir forma veya daha da az istenen bir füzyon sonrası forma dönüştüğünü keşfettiler. Ayrıntılı bir yapısal analiz, füzyon öncesi yapının merkezinde, birbirini iten üç pozitif yüklü molekülün bulunduğu “asidik bir yama” olduğunu ve en ufak bir bozulmada RSV F proteinini yaylı bir transformatör gibi açmaya hazır olduğunu ortaya koydu.
Zhu, “Bu, bir virüsün evrim sırasında anahtar proteininin hareketini kontrol etmek için edinebileceği inanılmaz bir özellik,” diyor. “Neyse ki, bunun üstesinden de gelebiliriz, ya kaba kuvvetle ya da daha iyisi, sorunun kaynağı olan asidik yamayı doğrudan ele alan akıllı bir mutasyonla.”
Zhu, RSV F proteinini merkezindeki bir çift molekülü değiştirerek yeniden tasarladı ve dışarıya doğru iten kuvveti çekici bir kuvvete dönüştürdü. Daha sonra, ekibi bu yeni F proteininin hem laboratuvarda daha kararlı olduğunu hem de fareleri RSV’ye karşı aşılamak için başarılı bir şekilde çalıştığını gösterdi.
Zhu, “Bu, diğer viral F proteinleri için de benzer bir yaklaşım sergileyebileceğimizi gösteriyor,” diyor. “En azından, aşıları tasarlarken yapılarında benzer itici yamalar arayabiliriz.”
Zhu, hMPV F proteininde aynı itici molekül parçasını bulamadı; bunun yerine, proteini bir arada tutmak için “kaba kuvvet” çözümü olarak güçlü bir kimyasal bağ kullandı. Bir kez daha, modifiye edilmiş protein aşı olarak bozulmadan kalacak kadar kararlıydı.
Zhu, gelecekteki çalışmalarda, son çalışmalarında bildirilen, RSV ve hMPV F proteinlerini insan vücuduna iletmek için kendi kendini birleştiren bir protein nanopartikül (SApNP) platformu kullanan deneysel bir aşı geliştirmeyi planlıyor. Zhu, “Bu, bizim yeni nesil RSV/hMPV kombo aşımız olacak,” diyor.
Kaynak ve devamına Buradan ulaşabilirsin.
