MIT bilim insanlarının keşfi, güçlü bir bağışıklık tepkisi sağlıyor ve potansiyel bir tümör aşısının geliştirilmesinde kullanılabilir.
Baş araştırmacılar Laura L. Kiessling , Jeremiah A. Johnson , Alex K. Shalek ve Darrell J. Irvine liderliğindeki dört MIT grubu ile MG Finn liderliğindeki Georgia Tech’teki bir grup arasındaki işbirliği, kanser hücrelerine karşı bağışıklık sistemi seferberliğini etkinleştirmek için yeni bir strateji ortaya koydu. Bugün ACS Nano’da yayınlanan çalışma , hem profilaktik hem de terapötik olarak bir tümör aşısı olarak işlev görmek için gereken tam olarak aynı tipte anti-tümör bağışıklığı üretiyor.
Kanser hücreleri, türetildikleri insan hücrelerine çok benzeyebilir. Buna karşılık, virüsler, bakteriler ve mantarlar, insan karbonhidratlarından belirgin şekilde farklı olan yüzeylerinde karbonhidratlar taşırlar. Dendritik hücreler (bağışıklık sisteminin en iyi antijen sunan hücreleri) yüzeylerinde, bu atipik karbonhidratları tanımalarına ve bu antijenleri içlerine getirmelerine yardımcı olan proteinler taşırlar. Antijenler daha sonra daha küçük peptitlere işlenir ve bir yanıt için bağışıklık sistemine sunulur. İlginç bir şekilde, bu karbonhidrat proteinlerinden bazıları bağışıklık yanıtlarını yönlendirmek için de iş birliği yapabilir. Bu çalışma, daha aktif, daha güçlü bir bağışıklık yanıtıyla sonuçlanan bu antijenleri dendritik hücrelere hedeflemek için bir strateji sunar.
Tümörlerin inatçılığıyla mücadele
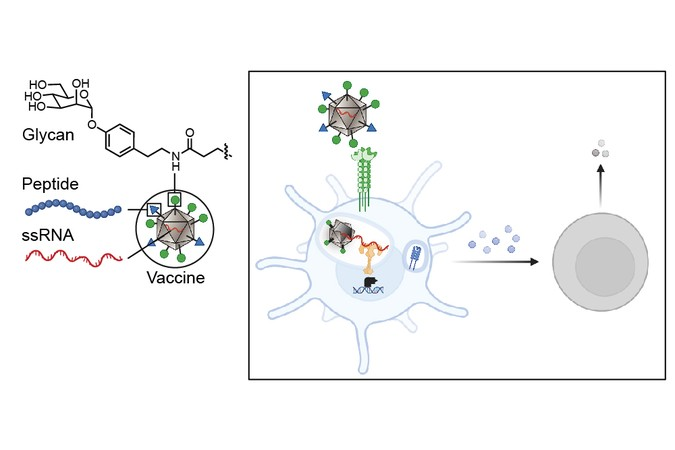
Araştırmacıların yeni stratejisi tümör antijenlerini yabancı karbonhidratlarla sarıyor ve bunları tek zincirli RNA ile birlikte iletiyor, böylece dendritik hücreler tümör antijenlerini potansiyel bir tehdit olarak tanıyacak şekilde programlanabiliyor. Araştırmacılar, dendritik hücre bağışıklığının bir aktivatörü olarak hizmet etme yeteneği nedeniyle lektin (karbonhidrat bağlayıcı protein) DC-SIGN’ı hedef aldılar. Virüs benzeri bir parçacığı (dahili RNA’sı virüsten olmadığı için bulaşıcı olmayan bir RNA parçası üzerine birleştirilmiş virüs proteinlerinden oluşan bir parçacık) DC bağlayıcı karbonhidrat türevleriyle süslediler. Ortaya çıkan glikan kostümlü virüs benzeri parçacıklar benzersiz şekerler sergiliyor; bu nedenle dendritik hücreler bunları saldırmaları gereken bir şey olarak tanıyorlar.
Makalenin kıdemli yazarı Kiessling, “Dendritik hücrelerin yüzeyinde, bakteri veya virüslerin yüzeyindeki şekerlerle birleşen ve bunu yaptıklarında zarı delerek geçen lektin adı verilen karbonhidrat bağlayıcı proteinler bulunur,” diye açıklıyor. “Hücrede, DC-SIGN virüse veya bakteriye bağlandığında kümelenir ve bu da içselleştirmeyi teşvik eder. Virüs benzeri bir parçacık içselleştirildiğinde, parçalanmaya başlar ve RNA’sını serbest bırakır.” Toll benzeri reseptör (RNA’ya bağlı) ve DC-SIGN (şeker dekorasyonuna bağlı), bağışıklık tepkisini etkinleştirmek için sinyal verebilir.
Dendritik hücreler yabancı bir istilanın alarmını çaldığında, tipik bir hedefsiz aşıyla beklenen bağışıklık tepkisinden önemli ölçüde daha güçlü olan sağlam bir bağışıklık tepkisi tetiklenir. Dendritik hücreler bir antijenle karşılaştığında, bağışıklık sistemindeki bir sonraki hücre olan T hücrelerine, dendritik hücrelerde hangi yolların aktive edildiğine bağlı olarak farklı tepkiler vermeleri için sinyaller gönderirler.
Kanser aşısı geliştirmenin ilerlemesi
Bu yeni araştırma doğrultusunda geliştirilen potansiyel bir aşının aktivitesi iki yönlüdür. İlk olarak, aşı glikan kılıfı lektinlere bağlanarak birincil bir sinyal sağlar. Daha sonra, toll benzeri reseptörlere bağlanma güçlü bir bağışıklık aktivasyonu ortaya çıkarır.
Kiessling, Finn ve Johnson grupları daha önce virüs benzeri parçacıkları süslemek için kullanıldığında hücresel bağışıklık tepkilerini yönlendiren sentetik bir DC-SIGN bağlayıcı grubu tanımlamıştı. Ancak bu yöntemin kanser karşıtı bir aşı olarak kullanılıp kullanılamayacağı belirsizdi. MIT ve Georgia Tech laboratuvarlarındaki araştırmacılar arasındaki iş birliği, bunun aslında mümkün olduğunu gösterdi.
MIT Polimerler ve Yumuşak Madde Programı’nda kimya alanında doktora yapan ve Kiessling ile Johnson laboratuvarlarının ortak üyesi olan Valerie Lensch, önceden var olan stratejiyi alıp bunu kanser karşıtı bir aşı olarak test etti ve bunu yapabilmek için immünoloji hakkında çok şey öğrendi.
Lensch, “Antijene özgü hücresel bağışıklık tepkilerini yönlendirmek için tasarlanmış modüler bir aşı platformu geliştirdik” diyor. “Bu platform yalnızca kansere karşı mücadelede önemli bir rol oynamakla kalmıyor, aynı zamanda sıtma parazitleri, HIV ve Mycobacterium tuberculosis gibi zorlu hücre içi patojenlerle mücadele için de önemli bir potansiyel sunuyor. Bu teknoloji, aşı geliştirmenin özellikle zorlu olduğu bir dizi hastalıkla mücadele için umut vadediyor.”
Lensch ve araştırmacı arkadaşları, başarı potansiyeli gösteren bir tasarım belirlemeden önce bu glikan kostümlü virüs benzeri parçacıkların kapsamlı yinelemeleriyle in vitro deneyler yürüttüler. Bu başarıldığında, araştırmacılar araştırmaları için heyecan verici bir dönüm noktası olan in vivo bir modele geçebildiler.
Kiessling Laboratuvarı’nda doktora sonrası araştırmacı olan Adele Gabba, Lensch ile birlikte in vivo deneyleri yürüttü ve doktora çalışmalarını Georgia Tech’te Profesör MG Finn ile birlikte yürüten Robert Hincapie, MIT’deki araştırmacılar tarafından kendisine gönderilen bir dizi glikan ile virüs benzeri parçacıkları oluşturdu ve dekore etti.
Gabba, “Karbonhidratların, hücrelerin iletişim kurmak ve bağışıklık sistemini yönlendirmek için kullandığı bir dil gibi davrandığını keşfediyoruz” diyor. “Bu dili çözmeye başlamamız ve artık onu bağışıklık tepkilerini yeniden şekillendirmek için kullanabilmemiz heyecan verici.”
Lensch, “Bu aşının arkasındaki tasarım prensipleri, uzun yıllar boyunca önceki lisansüstü öğrenci ve doktora sonrası araştırmacılar tarafından yürütülen kapsamlı temel araştırmalara dayanmaktadır ve lektin etkileşimini optimize etmeye ve lektinlerin bağışıklıktaki rollerini anlamaya odaklanmaktadır” diyor. “Bu kavramların çeşitli uygulamalarda terapötik platformlara dönüştürülmesine tanık olmak heyecan vericiydi.”
