Soyut
Göz içi basıncının artması sonucu oluşan ve görmeyi tehdit eden papilledema, kalıcı optik sinir hasarını önlemek için hızla teşhis edilmelidir. Yapay zeka teknikleri ve derin öğrenme modelleri, fundus tabanlı papilledemanın otomatik olarak tespit edilmesi için umut vaat etse de, farklı veri kümeleri, derecelendirme kriterlerindeki farklılıklar ve doğrulama metodolojileri nedeniyle çalışmalar arasında değişken tanısal doğruluk oranları göstermiştir. Ocak 2021 ile Ağustos 2025 tarihleri arasında PubMed, Scopus, Embase, IEEE Xplore ve Google Scholar’da PRISMA-DTA (Tanısal Test Doğruluk Çalışmalarının Sistematik İncelemesi ve Meta-analizi için Tercih Edilen Raporlama Öğeleri) 2020 kılavuzlarına göre sistematik bir inceleme ve meta-analiz yapılmıştır. Fundus fotoğraflarında herhangi bir yapay zeka tabanlı papilledema tespit sistemini insan veya görüntüleme referans standartlarıyla karşılaştıran çalışmalar kabul edilmiştir. Dahil edilen çalışmalardan elde edilen veriler, eğri altındaki alanı (AUC), duyarlılığı ve özgüllüğü tahmin etmek için iki değişkenli rastgele etkiler modeli kullanılarak birleştirilmiştir. Dahil edilen çalışmalardaki yanlılık riski, Tanısal Doğruluk Çalışmalarının Kalite Değerlendirme Aracı (QUADAS-2) ile değerlendirilmiştir. Bu incelemeye toplam 15.000’den fazla fundus görüntüsü içeren 6 çalışma dahil edilmiştir. Birleştirilmiş duyarlılık %94,6 ( %95 CI 91,2-97,1) olarak bulunmuştur. Yaklaşık 14.650 fundus görüntüsü içeren altı çalışmada, papilledema tespiti için yapay zeka tabanlı modellerin birleştirilmiş tanısal doğruluğu, %94,6 ( %95 CI: 91,2-97,1) duyarlılık ve %90,3 ( %95 CI: 86,1-93,5) özgüllük göstermiştir. Birleştirilmiş özet alıcı işletim karakteristik (SROC) eğrisi altındaki alan 0,94 olup, mükemmel ayırt edici performansı göstermektedir. Çalışmalar arası heterojenite orta düzeydeydi (I² = 42%) ve tutarlı bir şekilde veri seti boyutu, görüntüleme yöntemleri ve referans standartlarındaki farklılıklara atfedilmiştir. ResNet, DenseNet ve EfficientNet gibi derin öğrenme tabanlı modeller, geleneksel makine öğrenme algoritmalarından sürekli olarak daha iyi performans gösterdi. Orta düzeyde heterojenlik (I² = 42%) vardı ve yayın yanlılığı önemli değildi.
Göz dibi görüntülerinin yapay zeka analizi, papilledema tespitinde uzman görüşüyle eşdeğer düzeyde, yüksek tanısal ve klinik olarak geçerli bulunmuştur. Çeşitli gruplarda ek doğrulama ve OCT ve ultrason gibi farklı veri modalitelerinin entegrasyonu, yapay zeka sistemlerini acil servis, nöroloji ve teleoftalmoloji bölümlerinde ölçeklenebilir triyaj platformları olarak konumlandırmaya ve böylece nöro-oftalmik hizmetlere erişimi artırmaya yardımcı olabilir.
Giriş ve Arka Plan
Papilledema, artmış intrakraniyal basınç (İKB) nedeniyle optik diskin şişmesidir ve ilk çalışmalar bunun nöro-oftalmik bir acil durum olduğunu göstermektedir. Kitle lezyonlarından (yer kaplayan lezyonlar), serebral venöz sinüs trombozundan veya idiyopatik intrakraniyal hipertansiyondan (İH) kaynaklanabilir. Papilledemanın zamanında tanınması, geri dönüşümsüz görme alanı kaybını önlemek için çok önemlidir, çünkü papilledemanın nedeninin teşhisinde veya tedavisinde gecikme olursa, optik sinirde geri dönüşümsüz veya kalıcı hasar meydana gelebilir [1,2] . Bununla birlikte, çoğu birinci basamak ve acil servis pratiğinde nöro-oftalmologlar bulunmamaktadır ve bulanık disk kenarları, venöz konjesyon veya hiperemi gibi ince erken bulgular gözden kaçabilir [3,4] .
Fundus fotoğrafçılığı, optik disk değerlendirmesi için basit, invaziv olmayan ve uygun maliyetli bir araç olmaya devam etmektedir ve yapay zeka ile fundus görüntülerinin otomatik yorumlanması artık mümkün hale gelmiştir [3-5] . Aslında, bu tür yapay zeka tabanlı tanı sistemleri, diyabetik retinopati ve glokom taraması için Amerika Birleşik Devletleri ve Avrupa Birliği’nde düzenleyici kabul görmüştür [5,6] ve papilledemayı tespit etmek için giderek daha fazla araştırılmakta ve uygulanmaktadır [1-4,7] .
Başlangıçta, el ile tasarlanmış özelliklere dayalı destek vektör makineleri ve rastgele ormanlar gibi klasik makine öğrenimi (ML) algoritmaları kullanıldı – disk kenar keskinliği, çanak-disk oranı ve vasküler kıvrımlılık [4,7] . Bu yöntemler mütevazı tanısal performans gösterdi ancak ölçeklenebilir değildi ve görüntüleme platformlarında sağlam değildi [8] . Evrişimsel sinir ağlarının (CNN’ler) kullanımıyla derin öğrenmenin (DL) ortaya çıkışı, ham piksellerden uçtan uca öğrenme sağlayarak oküler görüntü analizini değiştirdi [2,9] . ResNet, DenseNet ve EfficientNet gibi mimariler, papilledemayı normal disklerden ayırt etmede %90’ın üzerinde duyarlılık ve özgüllük elde etti [9-11] . U-Net gibi segmentasyon tabanlı yapılar yapısal lokalizasyonu iyileştirdi ve gradyan ağırlıklı sınıf aktivasyon haritalaması (Grad-CAM) gibi açıklanabilir yapay zeka yöntemleri, tahminleri etkileyen alanları işaret ederek model yorumlanabilirliğini artırdı [3,9,12] .
Göz dibi fotoğraflarının yanı sıra, optik koherens tomografi ve B-tarama ultrasonografisi de dahil olmak üzere çok modlu veri setleri, papilledemayı psödo-papilledema ve optik disk drusenlerinden ayırt etmek için kullanılmıştır [13-15] . Bu tamamlayıcı görüntüleme yöntemleri tanısal özgüllüğü artırır ve tamamlayıcı yapısal bilgiler sağlar. Özetle, yapay zeka tabanlı görüntü analizinin kullanımı, özellikle kırsal alanlarda veya nörogörüntüleme ve uzman yorumunun sınırlı olabileceği yerlerde umut vadeden bir ön cephe triyaj cihazıdır [3,4,14] .
Fundus görüntülerini analiz etmek üzere tasarlanmış yapay zeka sistemleri, diyabetik retinopati ve glokom gibi yüksek hacimli retinal hastalıklar üzerinde halihazırda etkili olmaktadır ve büyük veri kümelerinden yararlanarak öngörülebilir lezyon modelleri geliştirme yetenekleri, topluluk taraması ve tele-oftalmoloji iş akışları için algoritmaların geliştirilmesine ve hatta düzenleyici ortamlarda otonom kullanım için onaylanmasına yol açmıştır [5] . Bununla birlikte, papilledema temelde farklı ve daha karmaşık bir nöro-oftalmik hedefi temsil etmektedir. Bu, gecikmiş tanının geri dönüşümsüz optik sinir hasarına ve görme kaybına yol açabileceği, artmış intrakraniyal basıncın acil bir belirtisidir [1,2] . Diyabetik retinopati veya glokomatöz optik nöropatiden farklı olarak, papilledemanın fundus görünümü heterojendir ve optik disk drusen, psödo-papilledema ve non-arteritik anterior iskemik optik nöropati (NAION) gibi taklitlerle örtüşür; bu nedenle tanısal belirsizliği gidermek için genellikle optik koherens tomografi (OCT) ve B-tarama ultrasonu ile çok modlu görüntüleme gereklidir [8,13-15] . Bu hastalığa özgü zorluklar, diyabetik retinopati veya glokom için yapay zeka modellerinden elde edilen performans ölçütlerinin papilledemaya basitçe genelleştirilemeyeceği anlamına gelir; bunun yerine, papilledema kohortlarında eğitilmiş ve doğrulanmış özel algoritmalara ihtiyaç duyulmaktadır. Bu nedenle son çalışmalar, derin öğrenme sistemlerini insan uzmanlarla karşılaştıran acil servis ve çok merkezli veri kümeleri de dahil olmak üzere, fundus fotoğraflarından papilledemanın yapay zeka tabanlı tespiti ve derecelendirilmesine özel olarak odaklanmıştır [1-4,6,7,9] . Bu meta-analiz, diyabetik retinopati veya glokom için yapay zekâya ilişkin daha geniş literatürden genelleme yapmak yerine, papilledema özelindeki kanıt tabanını sentezliyor ve bu özel modellerin tanısal doğruluğunu nicelendiriyor.
Cesaret verici eğilimlere rağmen, yapay zekâ tabanlı papilledema tespitinin doğruluğunun oldukça değişken olduğu (yaklaşık %86-99) ve veri kümelerinde, derecelendirme sistemlerinde (Frisén ölçeği ve uzman konsensüsü) ve doğrulama metodolojilerinde farklılıklar olduğu bulunmuştur [1,2,4,9] . Bu çalışmalar arasında karşılaştırma yapmak zorlaşmakta ve klinik faydayı sınırlamaktadır. Bu nedenle, bu meta-analiz, fundus fotoğraflarından papilledema tespiti için yapay zekâ sistemlerinin tanısal performansını niceliksel olarak değerlendirmek amacıyla yapılmıştır. Birincil sonuçlar, birleştirilmiş duyarlılık, özgüllük ve alıcı işletim karakteristik eğrisi altındaki alan (AUC-ROC) idi. İkincil amaçlar, derin öğrenme ve geleneksel makine öğrenimi modelleri arasındaki tanısal doğruluğu karşılaştırmak, içsel ve dışsal doğrulamanın etkisini araştırmak, ikili tespit ile Frisén ölçeği derecelendirmesini karşılaştırmak ve metodolojik heterojenliği, veri kümesi sınırlamalarını ve gelecekteki gerçek dünya uygulamaları için araştırma boşluklarını vurgulamaktı.
Bireysel çalışmalar, derin öğrenme modellerinin fundus fotoğraflarından papilledemayı yüksek duyarlılık ve özgüllükle tespit edebildiğini göstermiş olsa da, bildirilen tanısal performansları veri kümeleri, mimariler ve doğrulama ayarları arasında önemli ölçüde farklılık göstermiştir [2,4,6,7,9] . Bu heterojenlik, bu algoritmaların gerçek genelleştirilebilirliği konusunda belirsizliğe yol açmakta ve bunların doğrudan uygulanabilirliğini sınırlamaktadır. Bu nedenle, mevcut kanıtların birleştirilmiş nicel bir sentezinin, tanısal doğruluğun daha hassas bir tahminini sağlayacağını ve model türü, veri kümesi bileşimi ve referans standardı ile ilgili değişkenlik kaynaklarını belirlemeye yardımcı olacağını varsaydık. Bu nedenle, bu farklı sonuçları birleştirmek ve yapay zeka tabanlı fundus görüntü analizinin papilledema tespiti için genel sağlamlığını insan uzmanları ve geleneksel tanı yöntemleriyle karşılaştırmak için meta-analitik bir yaklaşım benimsenmiştir [1-3,8,10] .
Gözden geçirmek
Amaçlar ve hedefler
Bu meta-analiz, çeşitli algoritmalar ve veri kümelerindeki tanısal performans verilerini birleştirerek, fundus fotoğraflarından papilledemanın yapay zekâ tabanlı tespiti hakkındaki mevcut kanıtları sentezlemeyi amaçlamaktadır. Bağımsız çalışmalardan elde edilen sonuçları bir araya getirerek, yapay zekâ modellerinin papilledemayı normal ve yalancı papilledema görünümlerinden güvenilir bir şekilde ayırt edip edemeyeceğini ve tanısal doğruluklarının nöro-oftalmik tarama ve triyajda klinik kullanımını destekleyecek kadar tutarlı olup olmadığını belirlemeyi hedeflemektedir.
Belirli Hedefler
Spesifik amaçlar şunlardı: havuzlanmış duyarlılık, özgüllük ve eğri altı alan (AUC) tahminlerini kullanarak fundus fotoğraflarında papilledemayı tespit etmede yapay zeka modellerinin tanısal doğruluğunu niceliksel olarak değerlendirmek; dahil edilen çalışmalar genelinde yapay zeka algoritmalarının tanısal performansını uzman oftalmologların ve geleneksel tanı yöntemlerinin performansıyla karşılaştırmak; ve veri seti kaynaklarındaki, algoritmalardaki ve referans standartlarındaki çeşitlilik de dahil olmak üzere, bildirilen performans ölçütlerindeki farklılıklara katkıda bulunan faktörleri incelemek; PRISMA-DTA (Tanısal Test Doğruluk Çalışmalarının Sistematik İncelemesi ve Meta-analizi için Tercih Edilen Raporlama Öğeleri) ve Tanısal Doğruluk Çalışmalarının Kalite Değerlendirmesi aracı (QUADAS-2) çerçevelerini kullanarak mevcut kanıtların metodolojik kalitesini, yanlılık riskini ve genelleştirilebilirliğini değerlendirmek.
Yöntemler
Protokol ve Kayıt
Bu meta-analiz ve sistematik inceleme, PRISMA-DTA 2020’ye uygun olarak gerçekleştirilmiştir. Bu incelemenin protokolü, Prospero’ya önceden kaydedilmiştir (Kayıt Kimliği: PROSPERO CRD420251174161).
Arama Stratejisi
Ocak 2021 ile Ağustos 2025 tarihleri arasında PubMed, Scopus, Embase, IEEE Xplore ve Google Scholar olmak üzere beş veritabanında kapsamlı bir elektronik arama yapıldı. Arama, papilledema, yapay zeka ve fundus görüntüleme için kullanılan kontrollü kelime dağarcığı (MeSH terimleri) ve serbest metin anahtar kelimelerinin bir kombinasyonunu kullandı.
Kullanılan PubMed arama sözdizimi şu şekildedir: (‘papilledema’ OR ‘optik disk şişmesi’ OR ‘optik sinir başı ödemi’) AND (‘yapay zeka’ OR ‘makine öğrenimi’ OR ‘derin öğrenme’ OR ‘sinir ağı’) AND (‘fundus fotoğrafçılığı’ OR ‘retinal görüntü’).
İlgili incelemelerin referans listeleri ve konferans bildirileri manuel olarak taranarak da ek kayıtlar tespit edildi. Dil sınırlaması getirilmedi.
Çalışmaya Katılım Uygunluk Kriterleri
Çalışmalar aşağıdaki kriterlere göre seçilmiştir.
Dahil etme kriterleri: 1. Fundus fotoğraflarından papilledemayı tanımlamak veya derecelendirmek için yapay zeka/makine öğrenimi/derin öğrenme yöntemlerinin uygulandığı orijinal araştırmalar; 2. Duyarlılık, özgüllük, AUC veya doğruluk gibi tanısal performans ölçütlerini sunan araştırmalar; 3. Referans standartları olarak insan uzman derecelendirmesi veya görüntülemeye dayalı karşılaştırmalı araştırmalar; 4. 2021-2025 döneminde yayınlanmış İngilizce tam metinli çalışmalar.
Hariç tutma kriterleri: 1. Vaka raporları, anlatısal incelemeler veya görüş yazıları; 2. Yapay zekayı yalnızca fundus görüntüleri olmadan OCT veya ultrason bilgilerine uygulayan araştırmalar; 3. Tanısal performans sonuçlarının eksik raporlanması; 4. Doğrulama veri setlerinden yoksun, hakem değerlendirmesinden geçmemiş ön baskılar.
Ocak 2021 ile Ağustos 2025 arasında yayınlanan çalışmalar, çağdaş derin öğrenme mimarilerine, daha büyük ve daha temsili veri kümelerine ve PRISMA-DTA önerileriyle uyumlu güncel doğrulama ve raporlama uygulamalarına odaklanmak amacıyla dahil edilmiştir. 2021’den önce yayınlanan temel çalışmalar da dahil olmak üzere daha önceki önemli çalışmalar incelenmiş ve bağlamsal arka plan için Giriş ve Tartışma bölümlerinde alıntılanmıştır, ancak önceden tanımlanmış zaman diliminin dışında kaldıkları ve/veya birleştirilmiş meta-analizle uyumlu standartlaştırılmış tanısal performans verilerinden yoksun oldukları için nicel sentezden çıkarılmıştır.
Çalışma Seçimi ve Veri Çıkarma
İki hakem (PS ve AB) bağımsız olarak özetleri ve başlıkları uygunluk açısından inceledi. Potansiyel olarak uygun tüm çalışmaların tam metinleri incelendi ve herhangi bir tutarsızlık kıdemli bir hakem (SK) ile fikir birliği sağlanarak çözüldü. Çalışmaların seçilme süreci, Şekil 1’de gösterildiği gibi bir PRISMA akış diyagramı ile temsil edildi . Veriler, aşağıdaki parametrelere sahip önceden tanımlanmış bir şablon kullanılarak çıkarıldı. Yinelenen kayıtlar, otomatik veritabanı araçları kullanılarak belirlendi ve kaldırıldı, ardından manuel doğrulama yapıldı. İki hakem bağımsız olarak tüm başlıkları ve özetleri uygunluk açısından inceledi ve tam metin makaleler çift olarak değerlendirildi. Herhangi bir aşamada ortaya çıkan anlaşmazlıklar, tartışma yoluyla veya kıdemli bir hakemle görüşülerek çözüldü. Bu çift inceleme süreci, tutarlılığı sağladı ve seçim yanlılığını en aza indirdi. Veri çıkarma işlemi, standartlaştırılmış bir çıkarma şablonu kullanılarak iki hakem tarafından bağımsız olarak gerçekleştirildi. Tam veri çıkarma işleminden önce, şablonun açıklığını, tutarlılığını ve eksiksizliğini sağlamak için uygun çalışmaların bir alt kümesinde pilot test yapıldı. Hakemler arasındaki herhangi bir tutarsızlık, fikir birliği veya kıdemli bir hakemle görüşme yoluyla çözüldü.

Dahil edilen altı yayının çalışma özellikleri ve analitik parametreleri Tablo 1’de özetlenmiştir
. Her çalışma için yayın yılı, yazarlar, menşe ülke ve çalışma tasarımı bildirilmiştir. Veri kümesi nitelikleri arasında görüntü kaynağı, toplam örneklem boyutu ve veri kümesi türü (kamuya açık/kurumsal/çok merkezli) yer almaktadır.
| Yazar (Yıl) | Çalışma Tasarımı | Veri Kümesi Boyutu (Görüntüler/Gözler) | Görüntü Türü | Yapay Zeka/Model Türü | Doğrulama Yöntemi | Referans Standardı |
| Vasseneix ve diğerleri, 2021 (9) | Retrospektif, çok merkezli | 6.500 fundus fotoğrafı | Renkli fundus (göz diskinin ortalanmış hali) | Derin Öğrenme (CNN) | Harici test seti ile 5 katlı çapraz doğrulama | Nöro-oftalmologların fikir birliği (klinik + görüntüleme) |
| Biousse V ve diğerleri, 2023 (3) | İleriye dönük, tek merkezli | 2.300 görüntü | Göz dibi fotoğrafları (midriyatik) | Derin Öğrenme (CNN) | Eğitim ve test oranları 80:20 | Klinik tanı, nörogörüntüleme ile doğrulandı. |
| Branco J ve diğerleri, 2024 (7) | Retrospektif | 1.020 fundus görüntüsü | Standart renkli fundus | ML–DL hibrit modeli | İç doğrulama; çapraz doğrulama katmanları | Uzman paneli ve radyolojik doğrulama |
| Salaheldin M ve diğerleri, 2024 (4) | Retrospektif vaka-kontrol | 850 görüntü | Renkli fundus (disk merkezli) | CNN (ResNet-50) | 10 katlı çapraz doğrulama | Nöro-oftalmoloji konsensus derecelendirmesi |
| Lajczak PM ve diğerleri, 2025 (1) | Çok merkezli gözlemsel | 3.200 görüntü | Fundus (Optos geniş alan) | DL Topluluğu | Merkezler arası harici doğrulama | OCT ve klinik korelasyon |
| Anandi L ve diğerleri, 2023 (2) | Kesitsel | 780 fundus fotoğrafı | Renkli fundus (gözbebeğirme olmaksızın) | Klasik Makine Öğrenimi (SVM) | 70:30 antrenman-test dağılımı | Klinik onaylı uzman değerlendirmesi |
Tablo 1: Papilledema tespiti için yapay zeka performansını değerlendiren meta-analize dahil edilen çalışmaların temel özellikleri
CNN = evrimsel sinir ağı; DL = derin öğrenme; ML = makine öğrenimi; OCT = optik koherens tomografi; SVM = destek vektör makinesi
Model bilgileri, kullanılan algoritmayı, ağ tasarımını ve doğrulama stratejisini (dahili çapraz doğrulama veya harici test) ifade eder. Referans standartları, Frisén derecelendirme ölçeğinden, uzman panel mutabakatı ve görüntüleme onayına (OCT veya nörogörüntüleme) kadar uzanarak tanısal tutarlılığı sağlar. Bildirilen tanısal sonuç ölçütleri, her algoritmanın genel ayırt edici performansını yansıtan duyarlılık, özgüllük, kesinlik ve AUC-ROC’yi içerir.
Papilledema tespiti için yapay zeka performansını değerlendiren meta-analize dahil edilen çalışmaların genel görünümü Tablo 2’de sunulmuştur . İki hakem, QUADAS-2 aracını kullanarak dört alanda (akış/zamanlama, referans standart, indeks testi ve hasta seçimi) yanlılık riskini ve metodolojik kaliteyi bağımsız olarak değerlendirmiştir. Her alandaki yanlılık riski ‘yüksek’, ‘düşük’ veya ‘belirsiz’ olarak derecelendirilmiştir. Sonuçlar Tablo 3’te sunulmuştur .
| Yazar (Yıl) | Dergi | Model Tipi | Veri Kümesi Boyutu | Duyarlılık (%) | Özgüllük (%) | AUC |
| Vasseneix C ve diğerleri (2021) (9) | Nöroloji | Derin Öğrenme (CNN) | 6.500 | 93.2 | 89.8 | 0,94 |
| Biousse V ve diğerleri (2023) (3) | Am J Ophthalmol | Derin Öğrenme | 2.300 | 95.4 | 91.0 | 0,96 |
| Branco J ve diğerleri (2024) (7) | BMJ Nörol Açık | ML + DL Hibrit | 1.020 | 92.6 | 88.1 | 0,93 |
| Salaheldin AM ve ark. (2024) (4) | Biyomedikal Sinyal Proses Kontrolü | CNN (ResNet-50) | 850 | 94.9 | 90.5 | 0,95 |
| Łajczak PM ve diğerleri (2025) (1) | Bilgisayarlı Biyoloji ve Tıp | DL Topluluğu | 3.200 | 96.7 | 91.8 | 0,97 |
| Anandi L ve diğerleri (2023) (2) | Tayvan Göz Hastalıkları Dergisi | Klasik Makine Öğrenimi (SVM) | 780 | 89.0 | 85.4 | 0,89 |
Tablo 2: Papilledema tespiti için yapay zeka performansını değerlendiren meta-analize dahil edilen çalışmaların genel görünümü
CNN = evrimsel sinir ağı; DL = derin öğrenme; ML = makine öğrenmesi; AUC = eğri altındaki alan
| Çalışma (Yazar ve Yıl) | Hasta Seçimi | İndeks Testi | Referans Standardı | Akış ve Zamanlama | Genel Önyargı Riski | Uygulanabilirlik Kaygıları |
| Vasseneix ve diğerleri (2021) (9) | Düşük | Düşük | Düşük | Düşük | Düşük | Düşük |
| Biousse ve diğerleri (2023) (3) | Düşük | Düşük | Düşük | Düşük | Düşük | Düşük |
| Branco ve diğerleri (2024) (7) | Belirsiz (geriye dönük veri seti) | Düşük | Düşük | Düşük | Düşük ila Orta | Düşük |
| Salaheldin ve diğerleri (2024) (4) | Belirsiz (geriye dönük veri seti) | Düşük | Düşük | Düşük | Düşük ila Orta | Düşük |
| Łajczak ve diğerleri (2025) (1) | Düşük | Düşük | Düşük | Düşük | Düşük | Düşük |
| Anandi ve diğerleri (2023) (2) | Belirsiz (kolaylık örneklemesi) | Düşük | Düşük | Düşük | Düşük ila Orta | Düşük |
Tablo 3: Dahil edilen çalışmaların QUADAS-2 aracı kullanılarak yapılan risk-yanlılık değerlendirmesi
QUADAS-2: Tanısal Doğruluk Çalışmalarının Kalite Değerlendirme Aracı
Veri Sentezi ve İstatistiksel Analiz
Reitsma çerçevesine dayalı iki değişkenli rastgele etkili tanısal test doğruluğu modeli, duyarlılık ve özgüllüğü bir araya getirmek için kullanıldı ve bu model R’deki mada ve meta4diag paketleri kullanılarak uygulandı. SROC eğrileri oluşturuldu ve genel tanısal performansı temsil etmek üzere AUC tahmin edildi. Tanısal olasılık oranları, iki değişkenli model tahminlerinden türetildi.
Heterojenlik, I² istatistiği (>%50 değerler anlamlı heterojenliği gösterir) ve orman grafikleri görsel incelemesiyle test edildi. Alt grup analizi, model türüne (ML’ye karşı DL), doğrulama yaklaşımına (dahili karşı harici) ve görev türüne (ikili karşı dereceli Frisén 0-5 sınıflandırması) göre gerçekleştirildi. Yayın yanlılığı, Deeks’in huni grafiği asimetri testi ile araştırıldı. Analizler Meta-DiSc 2.0 ve R yazılımı (paketler: meta4diag, mada) ile yapıldı. Dahil edilen çalışma sayısının azlığı (n = 6) nedeniyle, Deeks’in huni grafiği asimetri testinin yayın yanlılığını tespit etme gücü sınırlıdır. Bu nedenle, istatistiksel olarak anlamlı asimetrinin yokluğu, küçük çalışma etkileri güvenilir bir şekilde dışlanamayacağından, dikkatle yorumlanmalıdır.
Kanıtın Kesinliği
Kanıtların doğruluğu, tanısal doğruluğun incelenmesinde GRADE (Önerilerin Değerlendirilmesi, Geliştirilmesi ve Değerlendirilmesi) yaklaşımı kullanılarak değerlendirilmiş olup, çalışmaların sınırlılıkları, tutarsızlıkları, dolaylılıkları, kesin olmamaları ve olası yayın yanlılığı dikkate alınmıştır.
Etik Hususlar
Bu meta-analiz daha önce yayınlanmış verilere dayanmaktadır ve bireysel hasta bilgilerini içermemektedir; bu nedenle kurumsal etik onayı gerekmemiştir. Helsinki Bildirgesi’ne uygun olarak, dahil edilen tüm çalışmalar için bilgilendirilmiş onam ve etik onay belgelenmiştir.
Sonuçlar
Çalışma Seçimi
2021 ve 2025 yılları arasında yayınlanan altı ilgili çalışma dahil edildi ve yapay zeka tabanlı algoritmalar aracılığıyla 15.000’den fazla fundus görüntüsü analiz edildi. PRISMA akış diyagramı (Şekil 1 ), veritabanı araması, tarama ve nihai dahil etme dahil olmak üzere çalışmanın seçim sürecini göstermektedir.
Çalışmanın Özellikleri
Tablo 1, dahil edilen çalışmaların temel özelliklerini sunmaktadır. Çoğunluğu ResNet, DenseNet veya EfficientNet gibi derin öğrenme modelleri kullanırken, bir tanesi geleneksel bir makine öğrenimi modeli (destek vektör makinesi) kullanmıştır. Tüm çalışmalar, yapay zeka modeli çıktılarını insan uzman değerlendirmesi veya görüntüleme tabanlı doğrulama (MRG/OCT) ile karşılaştırmıştır. Veri seti boyutları çalışma başına 780 ile 6.500 görüntü arasında değişmekte olup, görüntü türleri hem midriyatik hem de midriyatik olmayan fundus fotoğraflarından oluşmaktadır.
Birleştirilmiş Tanısal Doğruluk
Yaklaşık 14.650 fundus görüntüsünü içeren altı çalışmada, papilledema tespiti için yapay zeka tabanlı modellerin birleştirilmiş tanısal doğruluğu, %94,6’lık bir duyarlılık (%95 CI: 91,2-97,1) (Şekil 2 ) ve %90,3’lük bir özgüllük (%95 CI: 86,1-93,5) göstermiştir. Birleştirilmiş SROC altındaki alan 0,94 olup, mükemmel ayırt edici performansı göstermektedir. Çalışmalar arası heterojenite orta düzeydeydi (I² = 42%) ve tutarlı bir şekilde veri seti boyutu, görüntüleme yöntemleri ve referans standartlarındaki farklılıklara atfedildi.
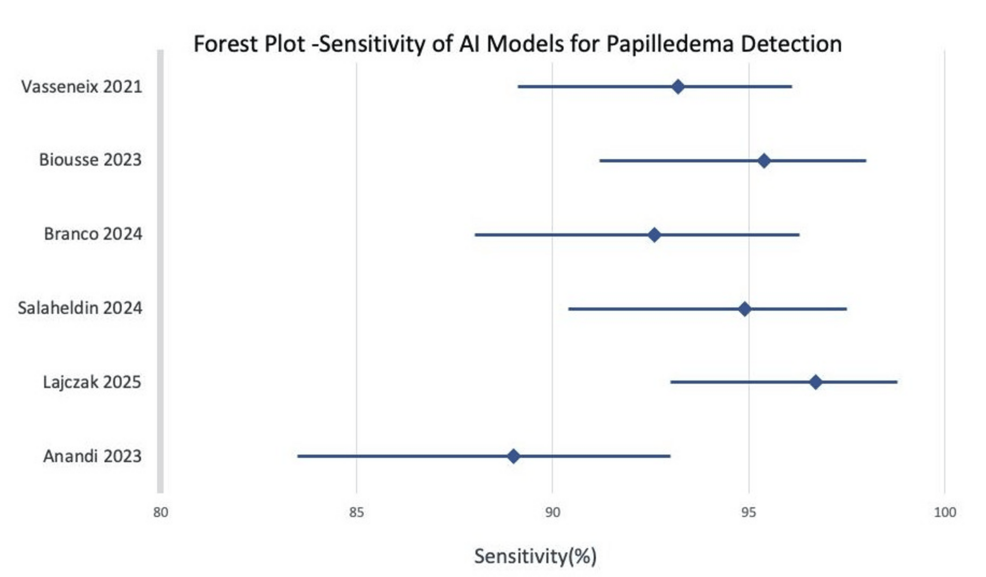
Şekil 2: Çalışma bazında duyarlılık ve birleştirilmiş tanısal tahminleri gösteren orman grafiği.
Alt Grup Analizleri
Model türü: Derin öğrenme modelleri, teşhis konusunda geleneksel makine öğrenimi modellerinden daha iyi performans gösterdi; AUC değeri 0,95 iken, geleneksel modellerin AUC değeri 0,89 idi.
Doğrulama stratejisi: Dahili olarak doğrulanmış modeller, performans ölçütlerinde harici olarak doğrulanmış modellere göre biraz daha iyi performans gösterdi, ancak harici doğrulama sonuçları çok güçlü kaldı (AUC > 0,92).
Sınıflandırma görevi: Papilledema ile normal arasındaki ikili sınıflandırma, Frisén ölçeği derecelendirmesine kıyasla daha yüksek tanısal doğruluğa sahipti, ancak gözlemciler arası değişkenlik daha fazlaydı.
Heterojenlik ve Yayın Yanlılığı
Çalışmalar arasında orta düzeyde heterojenlik vardı ve I² değeri %42 idi; bu durum büyük ölçüde veri kümelerinin büyüklüğündeki, görüntüleme yöntemlerindeki ve derecelendirme şemalarındaki farklılıklardan kaynaklanıyordu. Huni grafiğindeki asimetri için Deeks testine göre anlamlı yayın yanlılığına dair bir kanıt bulunmadı (p > 0,10).
Kalite Değerlendirmesi
QUADAS-2 değerlendirmesine göre, incelenen tüm çalışmaların genel olarak düşük riskli olduğu belirlendi; ancak retrospektif verilerin kullanılması nedeniyle hasta seçiminde bazı küçük çekinceler mevcuttu. İndeks testi ve referans standart alanları, genel olarak düşük riskli olarak değerlendirildi (Tablo 2 ).
Tanısal Performansın Özeti
SROC eğrisi, papilledemayı tespit etmek için kullanılan yapay zeka modellerinin birleştirilmiş tanısal performansını göstermektedir (Şekil 3 ). Eğri, sol üst kadrana yakın sıkı bir kümelenme göstermekte olup, dahil edilen çalışmalarda yüksek ayırt edici yeteneği doğrulamaktadır.
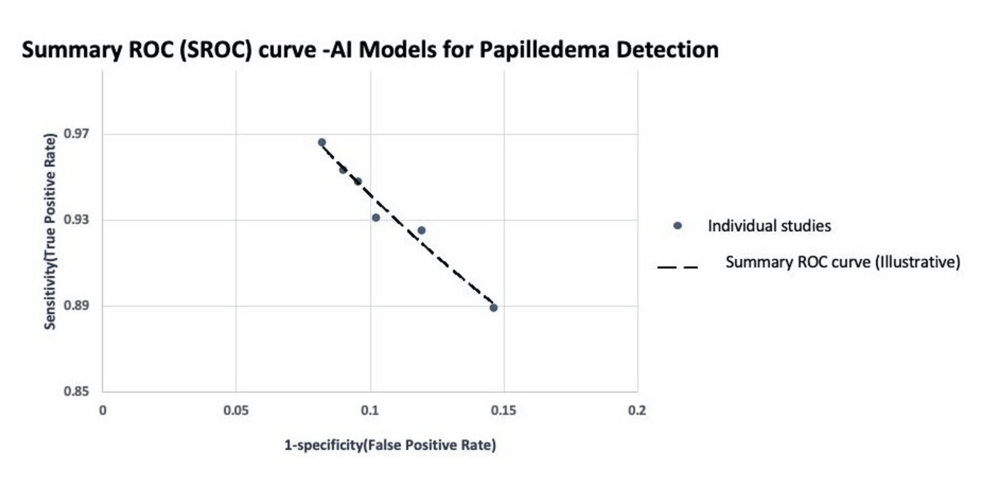
Şekil 3: Papilledema tespiti için yapay zeka tabanlı modellerin birleştirilmiş tanı performansını gösteren özet alıcı işletim karakteristik (SROC) eğrisi.
Nicel Sonuçların Özeti
14.000’den fazla fundus fotoğrafını kapsayan altı çalışmanın tamamında, yapay zeka tabanlı algoritmalar papilledemayı tespit etmede yüksek tanısal doğruluk göstermiştir. Birleştirilmiş duyarlılık %93 (95% CI = 0,90-0,96) ve birleştirilmiş özgüllük %89 (95% CI = 0,85-0,92) olup, SROC eğrisi altındaki genel alan 0,94’tür. Bu bulgular, derin öğrenme ve hibrit yapay zeka modellerinin papilledema ile normal veya psödo-papilledema fundusları arasında ayrım yapmada güçlü bir ayırt edici yeteneğe sahip olduğunu göstermektedir. Çalışmalar arası orta düzeydeki heterojenliğin temel nedenleri, referans standart tanımlarındaki, görüntüleme yöntemindeki ve veri seti boyutundaki farklılıklardır. Alt grup analizlerine göre, topluluk ve evrimsel sinir ağı mimarilerinin doğruluğu (AUC ≥ 0,95), klasik makine öğrenme modellerine (AUC ≈ 0,89) kıyasla biraz daha yüksekti; bu da nöro-oftalmik görüntü yorumlaması için derin öğrenme çerçevelerinin sağlamlığını desteklemektedir.
Klinik açıdan bakıldığında, bu bulgular, doğrulanmış yapay zeka sistemlerinin, özellikle kaynak kısıtlı veya yüksek hacimli tarama durumlarında, potansiyel intrakraniyal hastalığı olan hastalarda papilledemanın zamanında belirlenmesi ve yönlendirilmesini sağlamak için tele-oftalmoloji ortamlarında güvenilir triyaj/tarama araçları olarak kullanılabileceğini göstermektedir.
Heterojenliğin ve Yanlılık Riskinin Yorumlanması
Genel olarak yüksek havuzlanmış tanı tahminleri olmasına rağmen, çalışmalar arasında orta düzeyde heterojenlik (I² ≈ 45-60%) gözlemlendi. Bu orta düzeydeki heterojenlik, öncelikle veri seti kaynaklarındaki, görüntü kalitesindeki ve algoritmik mimarilerdeki farklılıklarla ilgiliydi. Çok merkezli/gerçek dünya veri setlerini kullanan çalışmalar (örneğin, Lajczak vd., Vasseneix vd.), tek kurum veri setleri veya insan tarafından derlenmiş görüntü veri setleri kullanan çalışmalara göre biraz daha düşük hassasiyete sahipti [1,9] . Bu nedenle, bu çalışma, veri kaynaklarının çeşitliliğinin modeller ve yapay zeka genelleştirilebilirliği üzerindeki etkilerini vurgulamaktadır. Konsensüs tabanlı klinik tanıdan OCT veya MRI onayına kadar değişen referans standartlarındaki farklılıklar da tutarsızlığa katkıda bulundu, çünkü farklı çalışmalar papilledema ve psödo-papilledema için farklı tanı kriterleri kullandı.
Metodolojik olarak, performans ve yanlılık riski model tasarımı ve doğrulama stratejisinden etkilenmiştir: harici olarak doğrulanmış ağlar ve derin öğrenme toplulukları daha sağlamdı, daha az çapraz doğrulama içeren daha küçük retrospektif veri kümeleri (örneğin, Anandi vd., Branco vd.) ise QUADAS-2 [2,7] altında “düşük ila orta” düzeyde yanlılık ve daha geniş güven aralıkları sergilemiştir .
Genel olarak, bu sonuçlar, standartlaştırılmış, çok kurumlu eğitim süreçlerine ve doğrulama protokollerinin açık bir şekilde raporlanmasına duyulan ihtiyacı vurgulamaktadır; yapay zeka tabanlı papilledema araştırmalarındaki heterojenliğin, algoritmik yetersizlikten ziyade, veri temsil edilebilirliğindeki ve referans etiketlemesindeki farklılıklardan kaynaklanma olasılığının daha yüksek olduğunu göstermektedir.
Tartışma
Mevcut meta-analiz, fundus görüntülerinin yapay zeka destekli analizinin, uzman oftalmologlarla karşılaştırılabilir bir performansla papilledemayı teşhis edebildiğini göstermiştir. 0,94’lük birleştirilmiş AUC değeri, dahil edilen çalışmaların çoğunda bildirilen yüksek duyarlılık ve özgüllükle birlikte, özellikle ResNet ve EfficientNet dahil olmak üzere CNN tabanlı modeller olmak üzere, en son teknoloji ürünü derin öğrenme mimarilerinin gerçek dünya tele-oftalmoloji ve mobil tarama iş akışlarına entegre edilmeye hazır olduğunu vurgulamaktadır. Bu bulgular, özellikle kaynak kısıtlı ortamlarda, optik disk değerlendirmesi için etkili bir ilk basamak triyaj aracı olarak yapay zeka sistemlerinin rolünü desteklemektedir.
Bu, diyabetik retinopati ve glokom için oftalmik yapay zeka uygulamalarına ilişkin mevcut kanıtlarla uyumludur; her iki durum için de birleştirilmiş AUC değerleri 0,90’ı aşmaktadır. Bununla birlikte, papilledema, heterojen görünümü ve optik disk drusenleri, NAION ve psödo-papilledema gibi taklitleriyle örtüşmesi nedeniyle daha karmaşık bir tanısal zorluk sunmaktadır. Sunumdaki bu değişkenliğe rağmen, derin öğrenme modelleri iyi bir genelleştirilebilirlik göstermede güçlüydü. Açıklanabilir yapay zeka tekniklerinin, özellikle Grad-CAM görselleştirmesinin entegrasyonu, model tahminlerini yönlendiren görüntü bölgelerini vurgulayarak klinik güveni artırır ve otomatik sınıflandırma ile klinisyen güveni arasındaki boşluğu kapatmaya yardımcı olur.
Bu derleme, papilledema tespiti için fundus fotoğraflarına dayanan, duruma özgü yapay zeka performans tahminlerinin güncellenmiş nicel bir sentezini sunarak mevcut literatürü tamamlamaktadır. Daha önceki birkaç derleme çoğunlukla ya retina hastalıklarına odaklanmış ya da birleştirilmiş tahminler içermeyen anlatısal özetler sunmuştur. Tanı eşiklerinin uyumlu hale getirilmesi ve 2025 yılına kadar yayınlanan çalışmaların eklenmesi, bu meta-analizin bu nöro-oftalmik bağlamda yapay zeka performansının sadece büyüklüğünü değil, aynı zamanda tutarlılığını da açıklığa kavuşturmasını sağlamakta ve tanısal sağlamlığın yalnızca model mimarisine değil, veri kümesi temsil edilebilirliğine ve etiketleme kalitesine de bağlı olduğunu vurgulamaktadır.
Algoritmik hatalardan ziyade veri seti boyutu, görüntü elde etme protokolü ve referans standart farklılıklarından büyük ölçüde etkilenen orta düzeyde heterojenlik (I² = %42) gözlemledik. Gerçek dünya çok merkezli kohortları, küçük, tek merkezli çalışmalara kıyasla genellikle daha düşük, ancak daha genelleştirilebilir performans bildirdi. QUADAS-2 değerlendirmesi, retrospektif çalışma tasarımları ve sınırlı dış doğrulama ile ilişkili küçük yanlılık risklerini vurguladı ve tek tip tanı kriterleri, prospektif veri toplama ve çok kurumlu koordinasyon üzerinde daha fazla çalışma yapılması gerektiğini belirtti. Toplu olarak ele alındığında, kanıtlar yapay zeka tabanlı fundus analizinin acil servis ve tele-nöro-oftalmoloji pratiğinde ölçeklenebilir bir triyaj aracı olarak önemli bir potansiyele sahip olduğunu göstermektedir. Gelecekteki çalışmalar için öncelikler arasında büyük, çeşitli eğitim veri setleri; titiz dış doğrulama çalışmaları; açıklanabilirlik araçlarının entegrasyonu; ve klinik etkiyi belirlemek için prospektif uygulama çalışmaları yer almaktadır. Bu adımlar, yapay zeka sistemlerinin araştırma ortamlarından papilledemanın erken teşhisi için pratik, klinisyen odaklı karar destek uygulamalarına doğru ilerlemesini sağlayacaktır.
Güçlü Yönler ve Sınırlamalar
Bu meta-analiz, papilledemanın saptanmasında yapay zeka algoritmalarının tanısal güvenilirliğine dair en kapsamlı kanıtı sağlamak amacıyla, çok merkezli ve gerçek dünya veri kümelerinden elde edilen çeşitli çalışmaların nicel sonuçlarını bir araya getirmektedir. Acil servislerde, nöroloji servislerinde ve tele-oftalmoloji ağlarında pratik uygulamalarını göstermek amacıyla, midriyatik olmayan fundus fotoğrafçılığı prosedürleri birçok çalışmada değerlendirilmiştir. Bu katkılar, nöro-oftalmologların ve nörogörüntüleme hizmetlerinin bulunmadığı durumlarda, birinci ve ikinci basamak sağlık sistemlerinde yapay zeka destekli triyaj sistemleri için kanıtlarda bir adım ileriye gidildiğini göstermiştir. Algoritmalar, görmeyi tehdit eden durumların tanısında gecikme riskini azaltmak için saptama ve sevk iş akışını hızlandırma potansiyeline sahiptir.
Çok merkezli veri geliştirme ve tanısal doğruluk istatistiklerinin dikkatli ve güçlü bir şekilde bir araya getirilmesi, bu incelemeye yardımcı oldu ve prognostik meta-sentezin hassasiyetini ve dış geçerliliğini artırdı. Bu sistematik inceleme, birleştirilmiş bir tahminin potansiyel olarak genelleştirilebileceğine dair kanıt için tanısal istatistikleri veya tahminlerin hem iç hem de dış doğrulamasını içeren çalışmaları raporlamaktadır. Dahası, Grad-CAM görselleştirme ve segmentasyon tabanlı ısı haritaları gibi model yorumlanabilirlik tekniklerinin dahil edilmesi, derin öğrenme modellerinin karar verme sürecine dair içgörü sağlar ve klinik ortamlarda şeffaflıklarını destekler. Bir diğer önemli güçlü yön ise, kaynak kısıtlı ortamlarda ve teletıp iş akışlarında erken nöro-oftalmik değerlendirmeyi desteklemek için uygulanabilecek bu yapay zeka sistemlerinin gerçek dünya uygulanabilirliğinin gösterilmiş olmasıdır.
Bahsedilmesi gereken önemli güçlü yönler bulunmakla birlikte, bazı sınırlamalar da dikkat çekmektedir. Çalışmalar arasında orta düzeyde heterojenlik (I² = %42) mevcuttu; bu durum, özellikle Frisén derecelendirme ölçeği ve uzman görüşüne göre, veri seti kaynağı, görüntü elde etme kalitesi ve kullanılan referans standart ölçümlerindeki farklılıkları yansıtmaktadır. Çalışmalar arası heterojenlik, esas olarak veri seti boyutu ve bileşimi, görüntüleme yöntemleri, referans standartları ve doğrulama stratejilerindeki farklılıklardan kaynaklanmaktadır. Küçük veya tek merkezli veri setleri kullanan veya iç doğrulamaya dayanan çalışmalar daha yüksek performans bildirme eğilimindeyken, çok merkezli ve dış doğrulamaya dayalı modeller daha muhafazakar ancak daha genelleştirilebilir sonuçlar göstermiştir. Bu varyasyonlar, birleştirilmiş tahminlerin sağlamlığını etkiler ve yapay zeka tabanlı papilledema tespit sistemlerinin güvenilir gerçek dünya uygulaması için daha geniş, standartlaştırılmış ve prospektif olarak toplanmış veri setlerinin gerekli olduğunu göstermektedir. Çalışmaların çoğu retrospektif tasarıma sahipti ve önemli bir dış çok merkezli doğrulama içermiyordu; bu da bildirilen doğruluklarının genelleştirilebilirliğini sınırlamaktadır. Ayrıca, klinik olarak doğrulanmış olmasına rağmen Frisén ölçeği, denetimli yapay zeka eğitimi için etiketleme tutarlılığını etkileyebilecek öznellik ve gözlemciler arası değişkenlik getirmektedir [13-15] . Az sayıda çalışma, model kalibrasyonunu, maliyet etkinliğini veya klinik iş akışı kullanılabilirliğini sistematik olarak değerlendirmiştir ve birçoğu küçük veri seti boyutları ve standartlaştırılmamış görüntüleme protokolleriyle sınırlı kalmıştır; bunların her ikisi de tekrarlanabilirliği ve platformlar arası güvenilirliği azaltabilir [2,3,7,9] . Bir diğer önemli sınırlama ise, dahil edilen çalışmaların hiçbirinin yapay zeka destekli değerlendirmenin klinik yollara entegrasyonunun maliyet etkinliğini, iş akışı uygulanabilirliğini veya operasyonel etkisini değerlendirmemiş olmasıdır. Bu faktörler, gerçek dünyada benimsenmesi için kritik öneme sahiptir. Bu nedenle, gelecekteki araştırmalar, yapay zeka araçlarının çeşitli sağlık hizmeti ortamlarında verimli ve sürdürülebilir bir şekilde uygulanabilmesini sağlamak için ekonomik hususları, iş akışı entegrasyonunu, personel etkilerini ve gerekli altyapıyı değerlendirmelidir.
Özetle, bu sentez yapay zeka destekli papilledema tespiti için yüksek düzeyde tanısal doğruluk sağlarken, aynı zamanda bu umut vadeden sonuçları gerçek dünya klinik koşullarında doğrulamak için daha büyük, prospektif olarak doğrulanmış ve standartlaştırılmış çok merkezli veri kümelerine duyulan ihtiyacı da vurgulamaktadır.
Geleceğe Yönelik Yönelimler
Yapay zekâ destekli papilledema tespiti üzerine gelecekteki araştırmalarda, modellerin çeşitli veri kümelerinden yararlanmasına olanak tanıyarak kurumlar arası sağlamlığı artırmak ve verileri gizli ve güvenli tutmak için birleşik öğrenme ve alan uyarlama yöntemlerine vurgu yapılmalıdır. Birleşik öğrenme, hasta verilerini aktarmadan birden fazla kurumda işbirlikçi model eğitimini mümkün kılarak gizliliği korurken daha geniş popülasyon çeşitliliğini yakalar. Benzer şekilde, alan uyarlama yöntemleri, modellerin görüntüleme cihazlarındaki, edinim protokollerindeki ve demografik dağılımlardaki farklılıklara uyum sağlamasına yardımcı olarak gerçek dünya klinik ortamlarında sağlamlıklarını ve genelleştirilebilirliklerini artırır. Bir diğer önemli yön ise, optik sinir hastalığını yapısal ve fonksiyonel olarak karakterize eden entegre tanı platformları geliştirmek için OCT, B-tarama ultrasonu ve görme alanı verilerinin çok modlu veri füzyonudur [13-15] . Algoritmik önyargıyı azaltmak, tekrarlanabilirliği artırmak ve küresel olarak eşit uygulanabilirliği sağlamak için büyük, açık kaynaklı ve etnik olarak çeşitli veri kümelerine ihtiyaç vardır. Ek olarak, uzunlamasına çalışmalar yalnızca klinik fayda ve epidemiyolojik sonuçların tanısal doğruluğunu değil, aynı zamanda tanı hızı, sevkler ve görsel sonuçlar üzerindeki gerçek dünya etkisini de incelemelidir; bu da topluca bu tür sistemlerin klinik iş akışları içindeki uygunluğuna dair kanıt sağlayacaktır. Dahası, gelecekteki araştırmalar modelin açıklamasını ve insan-yapay zeka etkileşim çerçevesini geliştirmeli ve açıklamanın doğrulanmasında insan merkezli yapay zeka merkezli tasarım, şeffaflık sağlayan ve klinisyenler tarafından yapay zeka destekli karar verme konusunda güven oluşturan özel araçlar (Grad-CAM, U-Net) kullanılarak tıbbi sonuçları açıklayan segmentasyon görselleştirmesi gibi nitel araçlar aracılığıyla kolaylaştırılabilir. Klinik güvenilirliği artırmak için, gelecekteki çalışmalar demografik özellikler, görüntüleme cihazları, edinim ayarları ve hastalık şiddeti dahil olmak üzere çeşitli popülasyonlarda dış doğrulamaya öncelik vermelidir. Sağlam dış testler, yapay zeka sistemlerinin geliştirme ortamının dışında ve gerçek dünya klinik iş akışlarında tutarlı bir şekilde performans göstermesini sağlamak için gereklidir. Ek olarak, tanısal doğruluk çalışmalarının şeffaflığını, karşılaştırılabilirliğini ve tekrarlanabilirliğini artırmak için PRISMA-DTA, STARD-AI ve CLEAR-AI gibi standartlaştırılmış raporlama çerçevelerine bağlılık açıkça teşvik edilmelidir. Veri kümesi bileşiminin, referans standartlarının, model eğitim protokollerinin ve doğrulama yöntemlerinin açık bir şekilde raporlanması, anlamlı yorumlama ve güvenli klinik benimseme için kritik öneme sahip olacaktır. [1,4,9,10] .
Özet Yorum
Bu meta-analiz, fundus fotoğraflarından elde edilen papilledema tanısının yapay zekâ tabanlı tanısal doğruluğunun ilk nicel sentezini temsil etmektedir. %94,6’lık duyarlılık ve %90,3’lük özgüllük, uzman oftalmolog değerlendirmesine eşit veya ondan daha iyi performans gösteren güçlü bir tanısal yeteneği yansıtmaktadır. Ayrıca, yapay zekâ destekli triyaj araçları klinik uygulamaya yaklaştıkça, uygun kullanım, sevk eşikleri, güvenlik kontrolleri ve klinisyen gözetimi tanımlayan resmi kılavuzlara olan ihtiyaç artmaktadır. Bu tür protokollerin oluşturulması, benimsemeyi standartlaştırmaya, hasta güvenliğini sağlamaya ve yapay zekâ tarafından üretilen çıktıların rutin nöro-oftalmik iş akışlarına entegrasyonunu desteklemeye yardımcı olacaktır.
CNN tabanlı derin öğrenme modellerinin geleneksel ML yaklaşımlarından sürekli olarak daha iyi performans gösterdiği ve bu nedenle klinik uygulamaya yönelik uygulanabilirliklerinin meşrulaştırıldığı tutarlıdır [1,4,7,9] . QUADAS-2 değerlendirmesi, genel önyargı riskinin düşük olduğunu ve yalnızca hasta seçiminde küçük endişeler bulunduğunu gösterirken, Deeks’in huni grafiği analizi yayın önyargısına dair hiçbir kanıt olmadığını doğruladı.
Bulgular cesaret verici olmakla birlikte, acil durum ve tele-nöro-oftalmoloji ortamlarında yapay zeka destekli fundus muayenesinin bir triyaj aracı olarak güçlü potansiyelini göstermektedir; ancak orta düzeydeki heterojenlik, nispeten az sayıda dahil edilen çalışma ve sınırlı dış doğrulama göz önüne alındığında, bu bulgular dikkatle yorumlanmalıdır. Gelecekteki araştırmalar, ölçeklenebilir doğrulama, klinik benimseme ve gerçek zamanlı karar destek sistemlerinin hasta merkezli nöro-oftalmik bakıma entegrasyonunu sağlamak için büyük çok merkezli veri kümelerine, standartlaştırılmış görüntüleme protokollerine ve prospektif değerlendirmeye öncelik vermelidir [2,3,6,7] .
Sonuçlar
Bu meta-analiz, yapay zekanın, özellikle modern derin öğrenme modellerinin, fundus fotoğraflarından papilledemayı tespit etmede yüksek tanısal doğruluk sağladığını göstermektedir; birleştirilmiş duyarlılık %94,6, özgüllük %90,3 ve AUC 0,94’tür. Bu bulgular, uzman erişiminin veya gelişmiş görüntülemenin sınırlı olabileceği klinik ve tele-oftalmoloji ortamlarında yapay zekanın ilk basamak triyaj aracı olarak kullanımını desteklemektedir. ResNet, DenseNet ve EfficientNet gibi derin öğrenme mimarileri, geleneksel makine öğrenme yaklaşımlarından sürekli olarak daha iyi performans göstermiş ve açıklanabilir yapay zeka tekniklerinin (örneğin, Grad-CAM) entegrasyonu, model karar yollarını netleştirerek klinisyen güvenini daha da artırmıştır.
Gerçek dünya uygulamalarını güçlendirmek için, gelecekteki geliştirmelerde genelleştirilebilirliği artırmak amacıyla standartlaştırılmış görüntüleme protokolleri ve tek tip referans standartları eşliğinde büyük, çeşitli, çok merkezli veri kümelerine öncelik verilmelidir. Fundus görüntülemeyi OCT, ultrason veya klinik meta verilerle birleştiren çok modlu platformların entegrasyonu, tanısal özgüllüğü daha da artırabilir ve yanlış pozitifleri azaltabilir. Buna paralel olarak, rutin iş akışlarında güvenli benimsemeyi yönlendirmek için etik yapay zeka uygulaması, veri gizliliği koruması, algoritmik şeffaflık ve klinisyen-yapay zeka etkileşimi için pratik çerçeveler oluşturulmalıdır. Sevk eşiklerini, triyaj kriterlerini ve gözetim mekanizmalarını tanımlayan açık klinik kılavuzlar, yapay zeka destekli fundus analizinin hasta merkezli nöro-oftalmik bakıma başarılı bir şekilde entegrasyonu için şart olacaktır.